Koncepcja środka utleniania, najsilniejsze, przykłady
- 5064
- 327
- Maksymilian Kępa
A Środek utleniający Jest to substancja chemiczna, która ma zdolność odejmowania elektronów od innej substancji (środka redukującego), która je przekazuje lub traci. Jest również znany jako środek utleniający do tego elementu lub związku, który przekracza atomy elektroonegatywne do innej substancji.
Po badaniu reakcji chemicznych wszystkie zaangażowane substancje i procesy występujące w nich należy wziąć pod uwagę. Do najważniejszych są reakcje ograniczające tlenek, zwane także redoks, które obejmują przenoszenie lub przeniesienie elektronów między dwoma lub więcej gatunkami chemicznymi.

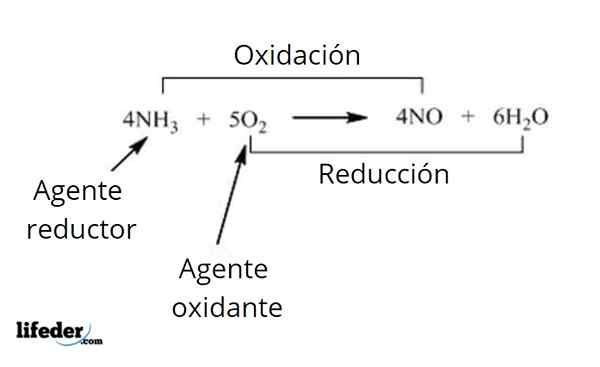
W tych reakcjach dwie substancje oddziałują: środek redukujący i środek utleniający. Niektóre z środków utleniających, które można obserwować częściej, to tlen, wodór, ozon, azotan potasu, perborowanie sodu, nadtlenki, halogeny i związki permangianowe, między innymi.
Tlen jest uważany za najczęstsze w środkach utleniających. Jako przykład tych reakcji organicznych, które obejmują przenoszenie atomów, wyróżnia się spalanie, które składa się z reakcji wytwarzanej między tlenem a innym materiałem utlewalnym.
[TOC]
Co to są środki utleniające?
W półprzestrzeniowym utlenianiu czynnik utleniający jest zmniejszony, ponieważ po otrzymaniu elektronów ze środka redukującego indukowane jest spadek wartości obciążenia lub liczby utleniania jednego z atomów środka utleniającego.
Można to wyjaśnić następującym równaniem:
2mg (s) + o2(g) → 2Mgo (S)
Można zauważyć, że magnez (mg) reaguje z tlenem (O2) i że tlen jest środkiem utleniającym, ponieważ odejmuje elektrony od magnezu - to znaczy jest zmniejszone - a magnez z kolei z kolei w z kolei w WHE czyn reakcyjny.
Może ci służyć: calcogeny lub amphumosPodobnie reakcja między silnym środkiem utleniającym a silnym środkiem redukującym może być bardzo niebezpieczna, ponieważ mogą one gwałtownie oddziaływać, więc muszą być przechowywane w osobnych miejscach.
Jakie czynniki definiują wytrzymałość środka utleniającego?
Gatunki te wyróżniają się według ich „siły”. Oznacza to, że najsłabsze są te, które mają niższą pojemność do odejmowania elektronów od innych substancji,.
Zamiast tego najsilniejszy mają większą łatwość lub pojemność do „uruchamiania” tych elektronów. W przypadku ich zróżnicowania rozważane są następujące właściwości:
Radio atomowe
Jest znany jako połowa odległości, która oddziela jądra od dwóch atomów od sąsiednich elementów metalowych lub „sąsiadów”.
Radia atomowe są ogólnie określane przez siłę, z którą najbardziej powierzchowne elektrony są przyciągane do rdzenia atomowego.
Dlatego promień atomowy elementu zmniejsza się w stole okresowym od dołu do góry i od lewej do prawej. Oznacza to, że na przykład lit ma znacznie większy promień atomowy niż fluorek.
Elektronialiczność
Electroneza jest definiowana jako zdolność atomu do przechwytywania elektronów należących do wiązania chemicznego dla siebie. Wraz ze wzrostem elektroony, pierwiastki mają rosnący trend, aby przyciągnąć elektron.
Ogólnie rzecz biorąc, elektroonegatywność wzrasta od lewej do prawej w stole okresowym i zmniejsza się, gdy rośnie charakter metaliczny, a fluor jest najbardziej elektroonegatywnym elementem.
Powinowactwo elektroniczne
Mówi się, że jest to zmienność energii rejestrowanej, gdy atom odbiera elektron do wygenerowania anionu; Oznacza to, że jest to zdolność substancji do odbierania jednego lub więcej elektronów.
Może ci służyć: aromatyczne podstawienie elektrofilowe: mechanizm i przykładyWraz ze wzrostem elektronicznego powinowactwa zwiększa się zdolność oksydacyjna gatunku chemicznego.
Energia jonizacji
Jest to minimalna ilość energii potrzebnej do uruchomienia elektronu z atomu lub, innymi słowy, jest miarą „siły”, z którą elektron jest powiązany z atomem.
Im większa wartość tej energii, odłączenie elektronu jest trudniejsze. Zatem energia jonizacji jest powiększona z lewej prawej i jest zmniejszona od góry do dołu w stole okresowym. W tym przypadku gazy szlachetne mają duże wartości energii jonizacji.
Najsilniejsze środki utleniające
Biorąc pod uwagę te parametry pierwiastków chemicznych, możliwe jest ustalenie, jakie są cechy, które muszą mieć najlepsze środki utleniające: wysoka elektrooniczność, w ramach radia atomowego i wysokiej energii jonizacji.
To powiedziawszy, uważa się, że najlepsze środki utleniające są zdolne do utleniania dużej liczby substancji.
Przykłady reakcji z środkami utleniającymi
W niektórych reakcjach redukcyjnych tlenku łatwiej jest wizualizować przenoszenie elektronów niż w innych. Niektóre z najbardziej reprezentatywnych przykładów zostaną wyjaśnione poniżej:
Przykład 1
Reakcja rozkładu tlenku rtęci:
2HGO (S) → 2HG (L) + O2(G)
W tej reakcji rtęć (środek utleniający) wyróżnia się jako odbiornik elektronów tlenu (środek redukujący), rozkładając się w ciekłym rtęci i tlenu gazowym podczas podgrzewania.
Może ci służyć: kwas láurowy: struktura, właściwości, zastosowania, korzyści, skutkiPrzykład 2
Kolejną reakcją, która jest przykładem utleniania, jest spalanie siarki w obecności tlenu w celu utworzenia dwutlenku siarki:
S (s) + o2(g) → SO2(G)
Tutaj można zauważyć, że cząsteczka tlenu jest utleniona (czynnik redukujący), podczas gdy elementarna siarka jest zmniejszona (środek utleniający).
Przykład 3
Wreszcie reakcja spalania propanu (stosowana w gazie do ogrzewania i kuchni):
C3H8(g) + 5o2(g) → 3co2(g) + 2h2Lub (l)
W tym wzorze można zaobserwować redukcję tlenu (środek utleniający).
Bibliografia
- Środek redukujący. Odzyskane z.Wikipedia.org
- Chang, R. (2007). Chemia, dziewiąta edycja (McGraw-Hill).
- Malone, L. J., I Dolter, T. (2008). Podstawowe pojęcia chemii. Odzyskane z książek.Google.współ.Iść
- Ebbing, d., I Gammon, s. D. (2010). Ogólna chemia, Enhanced Edition. Odzyskane z książek.Google.współ.Iść
- Kotz, J., Treichel, s. 1., I Towsend, J. (2009). Chemia i reaktywność chemiczna, ulepszone wydanie. Odzyskane z książek.Google.współ.Iść
- « Wysokie cechy górskie, pogoda, fauna, flora, lokalizacja
- Charakterystyka sztuki mezopotamskiej, malarstwo, rzeźba, ceramika »

