Transformacje materii
- 1525
- 293
- Estera Wojtkowiak
 Transformacje materii to transformacje, które cierpi bez zmiany jego składu. Na przykład woda w swojej cieczy, stałej (lodzie) lub sodzie (parowej) pozostaje woda
Transformacje materii to transformacje, które cierpi bez zmiany jego składu. Na przykład woda w swojej cieczy, stałej (lodzie) lub sodzie (parowej) pozostaje woda Jakie są transformacje materii?
Transformacje materii to zmiany, które cierpi bez zmiany składu. Oznacza to, że materia jest przekształcana, gdy przechodzi przez zmiany fizyczne i chemiczne.
Przykładami zmian fizycznych są tworzenie się lodu, gdy temperatura opada, rosa na liściach, które pojawiają się rano, rozszerzenie obiektów po podgrzaniu i magnetyzacja ciała.
Ze swojej strony utlenianie śrub i paznokci jest zmianą chemiczną, ponieważ tlenek jest substancją inną od oryginalnego żelaza. W każdym razie konieczne są zmiany energii, aby te transformacje miały miejsce.
Transformacja lodu to zmiana stanu, w którym woda zestala się, ale istnieje więcej możliwości. Materia występuje w naturze i w laboratorium w różnych stanach, z których gaz, ciekł i stał.
Ale ponieważ materia się zmienia, naukowcy napotykali więcej stanów o nieco egzotycznym charakterze, na podstawie eksperymentalnych i teoretycznych.
Można potwierdzić, że istnieje pięć podstawowych stanów materii:
- Solidny
- Płyn
- Gaz
- Osocze
- Kondensat Bose-Einstein
Spośród nich pierwsze trzy są stabilne w warunkach naszej planety, podczas gdy dwa ostatnie wymagają środków technologicznych, chociaż we wszechświecie są częste. Osocze jest w rzeczywistości najczęstszym stanem materii w kosmosie.
Podstawowe stany materii
W warunkach ciśnienia i temperatury Ziemi materia jest zwykle prezentowana w trzech stanach: stały, ciekł i gazowy, podczas gdy stany w osoczu i kondensatu Bose-Einsteina są uzyskiwane w różnych warunkach, które można osiągnąć w laboratorium.
Może ci służyć: niekonwencjonalne środkiAby wyjaśnić, dlaczego należy pamiętać, że materia składa się z cząstek, powiązanych przez siły, zarówno atrakcyjne, jak i odpychające. Siły przyciągania, jak sama nazwa wskazuje, mają tendencję do składania cząstek, podczas gdy odpychające mają odwrotny efekt.
Solidne, ciecze i gazy
Kiedy siły przyciągania panują między cząsteczkami, pozostają blisko siebie, razem w mniej lub bardziej ustalonych pozycjach Solidki. Cząstki mogą wibrować, ale nie porzucić swojej pozycji w stałym, dlatego utrzymuje to określony kształt i objętość.
w Płyny, Siły przyciągania pozwalają cząsteczkom kontynuować bliskość, ale są mniej intensywne niż w ciałach stałych, zapewniając im możliwość „poślizgnięcia się” się w określony sposób. Z tego powodu płyny dostosowują swój kształt do zawierającego je pojemnik, ale utrzymują stałą objętość.
Wreszcie w Gazy, Siły atrakcyjne są jeszcze słabsze, głównie siły odpychania. To sprawia, że cząstki pozostają od siebie z dala od siebie i przy znacznie większej swobodzie ruchu. Z tego powodu gazy rozszerzają się, aż dostępna objętość całkowicie zająć.
Kondensat i kondensat Bose-Einstein
Przez wystarczające podgrzewanie gazu, jony i elektrony oddzielają się w procesie zwanym jonizacja, W ten sposób osocze w laboratorium. Stan plazmowy nie jest łatwy do zobaczenia naturalnie w pobliżu Ziemi, ale można go zobaczyć z niego w północnych i południowych światłach.
To piękne naturalne zjawisko występuje, gdy cząstki wiatru słonecznego, raczej rozproszony plazma, wpływają na atmosferę Ziemi, jonizując.
Na drugim końcu skali, dużo chłodzenia, tuż nad bezwzględnym zero, pojawia się nowy stan materii, w którym większość cząstek znajduje się w stanie podstawowym, który jest najniższą energią.
Może ci służyć: najważniejszy aspekt małej nauki, wielka nauka i technologiiTen stan materii jest nazywany Kondensat Bose-Einstein, autorstwa fizyków Satyendra Bose i Albert Einstein, którzy przewidywali swoje istnienie w 1924 roku.
Wiele lat później, w 1995 r., Kilku naukowców udało się przenieść bardzo rozcieńczone gazy do tego stanu, łatwe zadanie, biorąc pod uwagę, że temperatury tylko nano-kelvina są wymagane powyżej bezwzględnego zera.
Zmiany stanu w sprawie
W naturze bardzo często zdarza się przechodzić z jednego stanu do drugiego. Zwykle te fizyczne zmiany są spowodowane zmianami ciśnienia i temperatury, pochodzące z wzrostu lub spadku energii cząstek.
Gdy energia cieplna jest dodawana do materiału, energia kinetyczna jej cząstek wzrasta, zmniejszając siłę przyciągania, która utrzymuje je w spójności. Jeśli materiał był w stanie stałym, może następnie przejść do stanu ciekłego, a nawet przejść bezpośrednio do stanu gazowego.
Przeciwnie, usuwając wystarczającą ilość energii cieplnej, możliwe jest przekształcenie materiału gazowego w ciecz lub przechodzi z cieczy na ciało stałe. W każdym razie skład substancji się nie zmienia.
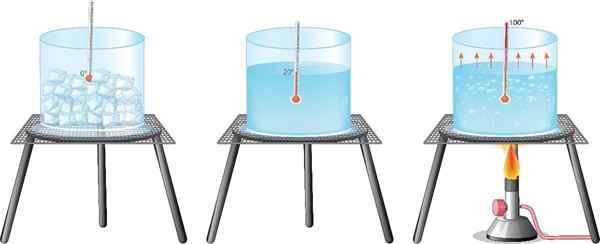
Najbardziej znanym przykładem dla wszystkich jest woda: dobrze wiadomo, że część ciekłej wody jest przekształcana w parę, gdy jest gotowana, podczas gdy przechodzi do lodu chłodząc do zamrażarki.
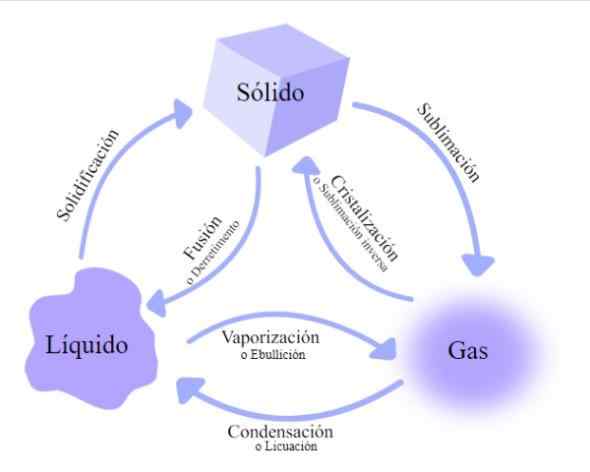 Zmiany w stanie materii. Źródło: Wikimedia Commons
Zmiany w stanie materii. Źródło: Wikimedia Commons Istnieje kilka kursów walutowych, przez które przechodzi materia, sklasyfikowane w zależności od tego, czy energia cieplna wzrasta lub zmniejsza się:
- Progresywny, Odbywają się, gdy materiał pochłania energię cieplną.
- Regresyjny, Są to te, które występują, gdy materiał daje energię.
Postępowe transformacje
Wśród różnych postępowych transformacji, które mają miejsce w tej sprawie poprzez dodanie energii, są:
Połączenie
Zmiana, która występuje, gdy materiał przechodzi z fazy stałej do fazy ciekłej. Na przykład, topiąc blok lodu, ciepło lub wosk na patelni.
Odparowanie
W tym przypadku sprawa jest przekształcana przez stan ciekł do stanu gazowego.
Może ci służyć: MetodologiaWaporyzacja występuje na dwa sposoby:
- Wrzenie, odbywa się, gdy materiał osiągnie temperatura wrzenia, W ten sposób energia wystarczy, aby przezwyciężyć siły międzycząsteczkowe, które utrzymują cząsteczki w ich stanie ciekłym. Każda substancja ma charakterystyczną temperaturę wrzenia, przy określonym ciśnieniu.
- Odparowanie, Tylko powierzchowne cząstki zmieniają stan, ponieważ materiał nie jest w temperaturze niezbędnej do wejścia do wrzenia. Najbardziej znanym przykładem jest odparowanie wody pozostawionej w pojemniku w temperaturze pokojowej.
Ulatnianie się
Nazywane też sublimacja, Odbywa się, gdy materiał przekształca się bezpośrednio z ciała stałego, bez przechodzenia przez fazę ciekłą.
Na przykład suchy lód to dwutlenek węgla2 Volatilized w temperaturze pokojowej. Naftalen, który służy do ochrony ubrań owadów, powoli przechodzi od solidnego do bycia gazem.
Jonizacja
Jest to przejście gazu plazmowego.
Przekształcenia regresywne
To transformacje spowodowane spadkiem energii cieplnej cząstek. Wśród nich są:
Zestalenie
Jest to zmiana materii ze stanu płynnego na substancję stałą przez chłodzenie, jak to się dzieje podczas umieszczania wody w zamrażarce. Proces jest taki, ponieważ substancja daje energię na zimno, tworząc lód.
Kondensacja
Występuje podczas przechodzenia ze stanu gazowego do fazy ciekłej, podobnie jak w przypadku pary wodnej w powietrzu, podczas nawiązania kontaktu z zimną powierzchnią przedniej szyby samochodu.
Skraplanie
Jest to transformacja materii podczas przechodzenia z gazu do cieczy, jak się zdarza, chłodzenie amoniaku lub dwutlenku węgla pod wysokim ciśnieniem.
Odwrotna sublimacja
Jest to przejście materii w stanie gazowym do stałego, jak w przypadku gazowego jodu, który zderza się z zimną powierzchnią, co powoduje powstawanie stałych kryształów. Jest również znany jako krystalizacja.
Desionizacja
Zmiana stanu w osoczu na stan gazowy.
Bibliografia
- Chang, R. (2013). Chemia. 11va. Wydanie. McGraw Hill Education.
- Giancoli, zm. (2006 =. Fizyka: zasady z aplikacjami. 6th. Ed Prentice Hall.
- Materia i jej właściwości. Odzyskane z: elbibliote.com.
- Opentax. Chemia. Źródło: OpenStax.org.
- Shipman, J. (2009). Wprowadzenie do nauk fizycznych. Dwunaste wydanie. Brooks/Cole, Cengage Editions.

