Tioles
- 3885
- 130
- Gabriela Łuczak
Tioles Są to związki organiczne, które mają grupę SH, zwaną tiol lub grupę sulfihydrilo. Jego ogólna formuła to RSH, jest w stanie reprezentować R na czynsz, aryl lub inna grupa chemiczna. Charakterystyczną cechą tolijów jest jego silny śmierdzący zapach.
Niektóre tusza są używane do przekazywania zapachu palnych gazów, aby wykryć wyciek tych gazów, które biorąc pod uwagę ich charakterystykę, może mieć wielkie niebezpieczeństwo. TIOLES są podobne do alkoholi, ponieważ mają grupę OH, podczas gdy tiole sh.
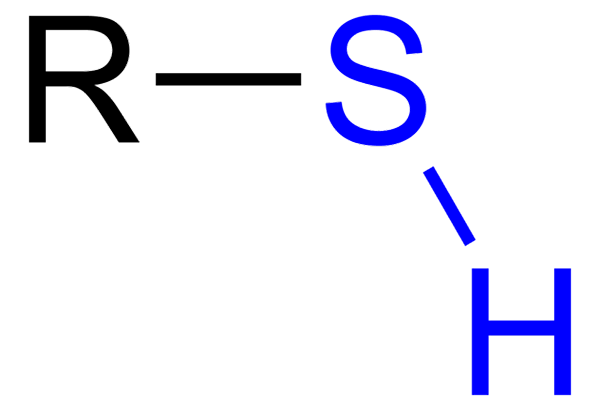
 Tiol z niebieską grupą sulfhydrillo
Tiol z niebieską grupą sulfhydrillo Jednak z kolei mają kilka różnic: grupa OH jest bardziej polarna niż grupa SH, a siarka jest mniejszym atomem niż.
To określa, że cząsteczki tuszu nie tworzą wiązań wodorowych ani wody ani wśród nich. Dlatego rozpuszczalność tuszów w wodzie jest niska, a jego temperatura wrzenia jest niższa niż w przypadku alkoholi z łańcuchem podobnych węgli.
TIOLES są szczególnie przydatne i częste w układach biochemicznych, ponieważ kilka odpowiada biomolekułom, takim jak koenzym. Jego wiązanie S-H jest bardziej kwaśne niż O-H, łatwiejsze do złamania, a także łatwiejsze do zastąpienia lub zastąpienia innych fragmentów molekularnych w licznej syntezy organicznej siarki.
[TOC]
Właściwości Tioles
 Śmierdzący aromat podnóża składa się głównie z tioli
Śmierdzący aromat podnóża składa się głównie z tioli Ogólne
Grupa alkoholi OH i grupa SH Tiole mają zestaw właściwości fizycznych i chemicznych dla przynależności tlenu i siarki do tej samej grupy chemicznej tabeli okresowej (przez grupę).
LOA Tioéters, Unicetals i Thioésters, które są analogiczne do związków chemicznych utworzonych przez alkohole, takie jak etery, acetal i estry. Jednak linki S-H i O-H przedstawiają pewne różnice, które będą odzwierciedlone we właściwościach tolijów i alkoholi.
Zapach
Charakterystyką dla tolinów o niskiej masie cząsteczkowej jest jego nieprzyjemny zapach, podobny do czosnku i cebuli. Ten zapach jest tak wielki, że ludzki zapach ma próg jednej części tiolu dla dziesięciu miliardów części powietrza.
Etanotiol jest dodawany do gazu ziemnego jako miara bezpieczeństwa, aby wykryć dowolną łatwopalną, ale sama toaleta ucieka. Zapach tolin zmniejsza się poprzez zwiększenie liczby węgli ich łańcucha, ponieważ zmienność i odsetek siarki tiolowej zmniejszają się.
Może ci służyć: fosforan amonu: struktura, właściwości, uzyskiwanie, zastosowaniaPunkt wrzenia i rozpuszczalność
Łącze S-H tolisów ma dipolowy moment mniejszy niż O-H link alkoholi. Ponadto atom siarki jest coraz mniejszy elektrooniczność niż atom tlenu.
To określa, że cząsteczki tuszu nie mogą tworzyć wiązań wodorowych z wodą lub wśród nich, co powoduje różnicę między fizycznymi właściwościami tolijów i alkoholi. Na przykład: metanotiol (cho3Sh) ma temperaturę wrzenia 6 ° C, podczas gdy metanol (Cho3Och) gotuje się w 65 ° C.
Dlatego w temperaturze pokojowej (25 ° C) metanol jest cieczą, a metanotyol to gaz.
Podsumowując: tusza mają niższą temperaturę wrzenia niż odpowiednie prezentowane alkohole. Z tych samych powodów rozpuszczalność tuszów w wodzie i w innych rozpuszczalnikach polarnych jest bardzo niska. Tymczasem alkohole o niskiej masie cząsteczkowej są bardzo rozpuszczalne w wodzie.
Reaktywność
Połącz S-H jest słabszy niż wiązanie O-H, więc łącze S-H łatwiejsza, co czyni tioli silnymi kwasami niż alkohole. Większość alkoholi ma PKA między 16 a 18.
To pozwala na toliole-): Bardzo silny środek nukleofilowy.
Grupa SH może utleniać się, tworząc połączenia disiarczkowe (-s-s-), które są obecne w utlenianiu glutationowym: tiol obecny w komórkach i ma funkcję przeciwutleniającą.
Bromo lub inne halogeny, a także tlen, mogą działać na tiol, tworząc mosty disulfurowe:
2 RSH +BR → R-S-S-R '+2 HBR
Związki RSSR są znane jako siarcze organiczne i alkiles, r2S.
Z drugiej strony silne środki utleniające, takie jak podchloryn sodu i nadtlenek wodoru, mogą działać na toliole, powodując kwasy sulfonowe:
Rsh +h2ALBO2 → RSO3H +3 H2ALBO
Nomenklatura
Nomenklatura IUPAC dla tolijów jest bardzo podobna do imienia alkoholi: nazwa alkano, z której dodaje się do niego sufiks „tiol”.
Zatem na przykład tatan pochodzący z Stano nazywa się 1-butanotiol, ch3Ch2Ch2Ch2SH, wskazując z liczbą pozycji grupy SH w węgle łańcucha.
Może ci służyć: kation: trening, różnice z anionem i przykładamiW ten sam sposób istnieje inna nomenklatura, znowu podobna do alkoholi: słowo „alkohol” zastępuje „Mercaptan” w imionach alkoholi. Na przykład Cho3SH, analog do alkoholu metylowego, CH3Och, nazywa się metyl lub mercaptan mercaptan.
Innym przykładem byłby Cho3Ch2CH (sh) ch3, Nazywany 2-butanotiol, secbutilic kupiec lub towary secbutil. To znaczy nacisk kładzie się na tożsamość R w formule RSH. Stąd inne normy nomenklatury dla alkoholi są również spełnione dla tioli.
I wreszcie, gdy grupa SH jest obecna w większej strukturze lub gdy dominują najważniejsze grupy, stosuje się przedrostek sulfihydrilo lub mercapto.
Na przykład związek CH3Ch2CH (sh) Coch3 Nazywa się to 3-Mercapto-2-penona. Należy zauważyć, że SH ma mniejsze priorytet niż grupy natlenione (z wyjątkiem eteru), więc drobne cyfry odpowiadają mu.
Synteza
Metoda syntezy tioli polega na reakcji tioty z halogenkiem alkilowym, który wytwarza sól pośrednich izotiouron. Jest to hydrolizowane przez wodorotlenek sodu w celu uzyskania tiolu i mocznika.
Ch3SH przygotowuje się przemysłowo przez reakcję siarkowodoru z metanolem, w obecności katalizatorów kwasowych:
Ch3Och +h2S → CH3Sh +h2ALBO
W innej metodzie produkcyjnej halogenku alkilowe reaguje się z hydrosulfuro sodu:
RX +Nash → Rsh +Nax
Aplikacje
Enzym naprawianie powiązanych z nanocząstkami
TIOLES są stosowane jako mosty do łączenia kompleksów nanocząstek-enzymów z złotymi elektrodami. Na przykład tusza są używane do utrwalenia kompleksu nanocząstek-uricasa, enzymu, który interweniuje w konwersji kwasu moczowego do allantoiny.
Reakcja tiol -no
Jest to reakcja organiczna między tiol a alkenem, nazywając reakcję „kliknij”; Że między innymi cechy jest to reakcja o wysokiej wydajności, szeroki zakres, który tworzy eliminowalne przez -produkty metodami niechromatograficznymi, a także łatwe do wykonania.
Reakcja tiol -no ma zastosowanie w syntezie tioazúcar: cukier obecny w salicynolu, inhibitorze α -glikozydazy. Salicynol został wyizolowany z roślin stosowanych na Sri Lance i Indiach w leczeniu cukrzycy.
Ponadto reakcja tiol -no stosuje się w chemii węglowodanów, polimeryzacji, chemii powierzchni, chemii syntezy i chemii peptydów.
Może ci służyć: punkt zamrożenia: jak to obliczyć i przykładyZapachy
 Gaz kuchenny to toaleta, ale dzięki składowi tioli o niskiej masie cząsteczkowej ma charakterystyczny zapach
Gaz kuchenny to toaleta, ale dzięki składowi tioli o niskiej masie cząsteczkowej ma charakterystyczny zapach Alifatyczne tusza o niskiej masie cząsteczkowej są włączone do gazów ziemnych, aby ich silny zapach służył jako ostrzeżenie w obliczu ucieczki lub wycieku gazu.
Medycyna
Penicylamina (c5HjedenaścieNIE2S) Jest to lek stosowany w leczeniu choroby Wilsona i reumatoidalnego zapalenia stawów.
I kaptopril (c9HpiętnaścieNIE3S), z drugiej strony, jest stosowany w leczeniu nadciśnienia tętniczego i zastoinowej choroby serca.
Oba są przykładami tolijów z aplikacjami leczniczymi.
Biologiczny
Grupy Tiole są obecne, wśród innych związków z funkcją biologiczną, w cysteinie, koenzymie A i glutationu.
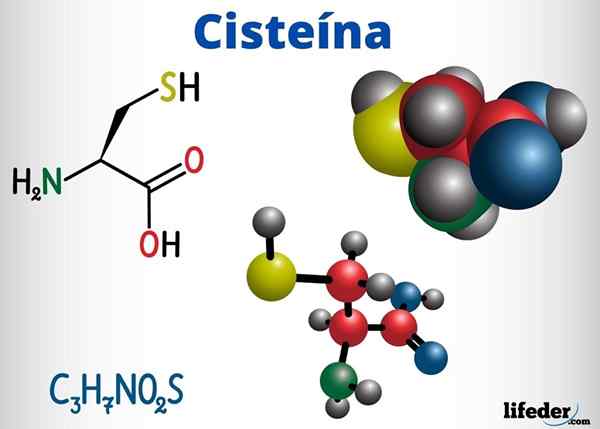
Cysteina jest aminokwasem zdolnym do tworzenia mostów disulfurowych w łańcuchu białka, a zatem odpowiedzialna za trzeciorzędową strukturę białka. Może również tworzyć mosty disulfurowe między różnymi łańcuchami białkowymi, powodując czwartorzędową strukturę białek.
Cysteina znajduje się w aktywnych ośrodkach licznych enzymów, a także ma działanie przeciwutleniające.
Glutation jest bardzo ważnym działaniem wewnątrzkomórkowym przeciwutleniającym, nadając ochronę komórek i makrocząsteczkom, które ją tworzą.
Z drugiej strony koenzym A jest tiolem, który interweniuje w syntezie i utlenianiu kwasów tłuszczowych. Ponadto koenzym pod postacią acetylokenzymu A, interweniuje na początku cyklu kwasu cytrynowego lub cyklu Krebsa.
Przykłady
Wreszcie niektóre nazwy tuszu będą wymienione w towarzystwie ich wzorów molekularnych:
-Kwas tiooctowy (c2H4TY)
-Koenzym a (cdwadzieścia jedenH36N7ALBO16P3S)
-Zmniejszona lśnienie (c10H17N3ALBO6S)
-Cysteina (c3H7NIE2S)
-Mercaptanol (c2H6TY)
-Metanotyol (rozdz3CII)
-1-propanotyol (c3H7CII)
-Butanotiol (c4H 9CII)
-Tiofenol lub tiomerosal (c6H6S)
-Pomelo mercaptano (c10H18S)
-Heksadekanotyol (c6H3. 4S)
-Penicylamina (c6HjedenaścieNIE2S)
-Captopril (c9HpiętnaścieNIE3S)
-Etanotiol (c2H6S)
-2-propenenetiol (c3H6S)
-Α-liPoic lub lipoamid (c8H14ALBO2S2). Jest to cykliczny disiarczk.
Bibliografia
- Graham Solomons t.W., Craig b. Fryhle. (2011). Chemia organiczna. (10th Wydanie.). Wiley Plus.
- Carey f. (2008). Chemia organiczna. (Szósta edycja). MC Graw Hill.
- Morrison i Boyd. (1987). Chemia organiczna. (Piąta edycja). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Tiol. Źródło: w:.Wikipedia.org
- Dr. Dietmar Kennepohl i in. (13 września 2020). Tiole i siarczki. Chemia librettexts. Odzyskane z: chem.Librettexts.org
- Redaktorzy Enyclopaedia Britannica. (2020). Tiol. Odzyskane z: Britannica.com
- Nolan MD i Scanlan EM (2020) Zastosowanie chemii tiol-enu w zakresie nauki peptydowej. Przód. Chem. 8: 583272. Doi: 10.3389/fchem.2020.583272
- Dr. Carl c. Wamser. (1999). Rozdział 9: alkohole i tiole. Źródło: Web.PDX.Edu

