Struktura siarczku wapnia (CAS), właściwości, uzyskiwanie, zastosowania
- 4404
- 1401
- Maksymilian Kępa
On Siark wapnia Jest to nieorganiczna substancja stała utworzona przez pierwiastek wapnia (Ca), a element (element) siarki, wzoru chemicznego to CAS. Jest to żółtawo -biały rozpuszczalny stał w wodzie, który występuje w naturze w niektórych wulkanach i w niektórych meteorytach w postaci minerału zwanego oldamimie.
CAS podczas rozpuszczania się w wodzie tworzy różne związki, ponieważ jon siarki s2- staje się sh- i jony OH są tworzone-. Powstały roztwór jest alkaliczny. Związek ten jest stosowany jako podstawa dla związków luminescencyjnych lub które wytwarzają światło widzialne w określonych warunkach. Materiały te są również używane w lekkich obrazach.
 W niektórych meteorytach znaleziono siarkę wapnia CAS. Autor: рote жравёё. Źródło: Pixabay.
W niektórych meteorytach znaleziono siarkę wapnia CAS. Autor: рote жравёё. Źródło: Pixabay. CAS uznano za możliwy lek do leczenia problemów serca i naczyń krwionośnych, takich jak nadciśnienie lub wysokie ciśnienie, która jest chorobą, która dotyczy dużej części populacji świata.
Z siarczkiem wapnia można uzyskać inne związki, takie jak azotan wapnia i węglan wapnia. Musi być obsługiwana ostrożnie, a w kontakcie z wilgocią atmosfery może wytwarzać h2S, który jest bardzo toksyczny.
[TOC]
Struktura
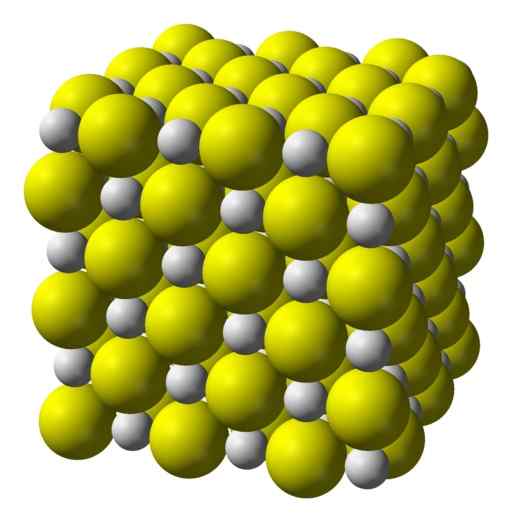
Siarczek wapnia jest silnie jonowym związkiem utworzonym przez jon wapnia CA2+ i jon siarczkowy s2-.
Krystalizuj w strukturze sześciennej, takiej jak sól skalna.
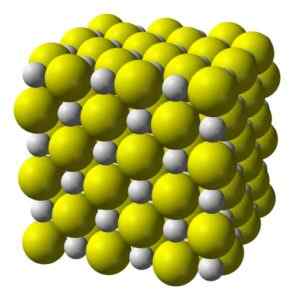 Sześcienna struktura krystaliczna siarczku wapnia. Żółty = siarka; Biały = wapń. Benjah-BMM27 / Public Domena. Źródło: Wikimedia Commons.
Sześcienna struktura krystaliczna siarczku wapnia. Żółty = siarka; Biały = wapń. Benjah-BMM27 / Public Domena. Źródło: Wikimedia Commons. Nomenklatura
- Siark wapnia
Właściwości fizyczne
Stan fizyczny
Żółtawo białe krystaliczne stałe, sześcienne kryształy, takie jak chlorek sodu.
Waga molekularna
72 144 g/mol
Temperatura topnienia
2528 ºC
Gęstość
2,59 g/cm3
Rozpuszczalność
Rozpuszczalny w wodzie. Nierozpuszczalne w etanolu.
Właściwości chemiczne
Roztwór wodny
Podczas rozpuszczania się w wodzie CAS jest podzielony na jony wapnia Ca 2+ i siarczek s2-. Ten ostatni w wodzie przyjmuje proton i staje się jonem hydrosulfuru SHH- uwalnianie jonu hydroksylowego OH-.
Może ci służyć: SiftedS2- + H2Lub ⇔ sh- + Oh-
Dlatego roztwory siarczku wapnia są alkaliczne (mają podstawowe pH) i nie mają jonów S2- Ale sh-.
Tylko w przypadku dodania dużej ilości alkaliów do roztworu, takiego jak wodorotlenek sodu NaOH. Bilans przesuwa się w kierunku tworzenia jonów siarki2-.
 Siark wapnia rozpuszcza się w wodzie tworzących inne związki. Autor: Clker-Free-Vector-Images. Źródło: Pixabay.
Siark wapnia rozpuszcza się w wodzie tworzących inne związki. Autor: Clker-Free-Vector-Images. Źródło: Pixabay. Sh- Możesz wziąć kolejnego protonu h+ wody, tworząc siarkowodór, który jest bardzo toksycznym związkiem.
CII- + H2Lub ⇔ h2S + OH-
Dlatego niewielkie ilości h w wodzie2S i narażone na wilgotność środowiska, CAS wydziela nieprzyjemny zapach typowy dla siarczku wodoru.
Związki obecne podczas rozpuszczania się w wodzie
Wynikiem wcześniej wskazanych reakcji wody jest to, że powstaje Ca (SH)2, CA (OH)2 i Ca (sh) (OH).
Cas + H2O → Ca (sh) (OH)
Ca (sh) (oh) + h2O → Ca (OH)2 + H2S
Reakcja kwasowa
Te same reakcje występujące w wodzie sprawiają, że CAS reaguje z kwasami tworzącymi h2S.
CAS + 2 HCl → CACL2 + H2S
Inne reakcje
Jeśli podgrzewa się roztwór siarczku wapnia z siarką, otrzymuje się jony polisiarczku42- i s32-.
Jeśli CAS jest podgrzewany w suchym powietrzu lub czystym tlenu, związek jest utleniony do obudowy siarczku wapnia3 A następnie do przypadku siarczanu wapnia4:
2 Cas + 3 O2 → 2 przypadek3
2 przypadek3 + ALBO2 → 2 przypadek4
Z środkami utleniającymi, takimi jak chloran potasu KCLO3, Azotan potasu KNO3 lub ołowiu dwutlenku2 Występują gwałtowne reakcje.
Uzyskanie
Siark wapnia można przygotować przez kalcynowanie (ogrzewanie w bardzo wysokiej temperaturze) wapń (CA) i siarki w obojętnej atmosferze, to znaczy nie są obecne na przykład tlenu lub pary wodnej.
Może ci służyć: kwas chloro (HCLO2)CA + S + ciepło → CAS
Można również uzyskać przez ogrzewanie obudowy siarczanu wapnia4 Z węglem:
Sprawa4 + 2 C → CAS + 2 CO2
Jednak w tym drugim przypadku nie jest uzyskiwany czysty dom, ponieważ reaguje dodatkowo z obudową4 tworząc Cao i tak2.
CAS jest również wytwarzany przez spalanie odpadów węglowych.
Obecność w naturze
CAS jest naturalnie obecny w minerałach Oldhamite. Jest to składnik niektórych meteorytów i jest ważny przez badania naukowe przeprowadzane w układzie słonecznym.
Uważa się, że Oldamihamita została utworzona przez kondensację w mgławicy, która powstała w układzie słonecznym. Jest również obecny w wulkanach.
 Siark wapnia CAS znajduje się w minerałach oldamihitowych, które znaleziono w niektórych meteorytach. Leon Hupperichs/CC BY-SA (https: // creativeCommons.Org/licencje/by-sa/3.0). Źródło: Wikimedia Commons.
Siark wapnia CAS znajduje się w minerałach oldamihitowych, które znaleziono w niektórych meteorytach. Leon Hupperichs/CC BY-SA (https: // creativeCommons.Org/licencje/by-sa/3.0). Źródło: Wikimedia Commons. Ponadto, siarczk wapnia jest naturalnie wytwarzany przez redukcję przypadku4 (tynk) prawdopodobnie przez działanie bakterii.
Aplikacje
W materiałach lekkich
Jedno z najbardziej rozpowszechnionych zastosowań siarczku wapnia była podstawą dla światła. Są to substancje, które emitują światło widzialne w pewnych okolicznościach.
W związkach luminescencyjnych CAS działa to jako podstawa i aktywatory są dodawane do struktury, takich jak chlorki niektórych elementów, takie jak cerio (CE3+) i Europio (UE2+).
Materiał wynikający z Unii CAS i aktywatora jest używany, na przykład na ekranach rur Ray Cathode, które składają się na stare ekrany komputerów lub komputerów lub starych urządzeń telewizyjnych.
 Monitory starożytnych komputerów miały rurki promieniowe katodowe, w których czasami stosowane są luminescencyjne związki siarczku wapnia i aktywatory. Autor: Andreas160578. Źródło: Pixabay.
Monitory starożytnych komputerów miały rurki promieniowe katodowe, w których czasami stosowane są luminescencyjne związki siarczku wapnia i aktywatory. Autor: Andreas160578. Źródło: Pixabay. Są one również stosowane w obecnych lampach diod emitujących światło lub LED (akronim dla angielskiego Diody emitujące światło).
Może ci służyć: Ayaroína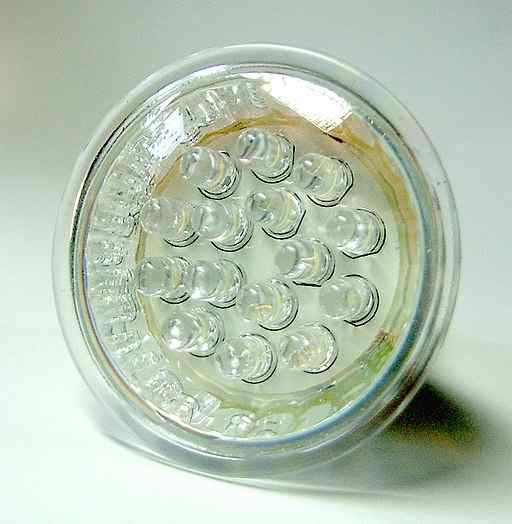 Lampa LED. Niektóre mogą zawierać luminescencyjne związki siarczku wapnia. Nie dostarczył autora, który można odczytać w maszynie. Apper założył (na podstawie roszczeń dotyczących praw autorskich). /CC BY-SA (http: // creativeCommons.Org/licencje/by-sa/3.0/). Źródło: Wikimedia Commons.
Lampa LED. Niektóre mogą zawierać luminescencyjne związki siarczku wapnia. Nie dostarczył autora, który można odczytać w maszynie. Apper założył (na podstawie roszczeń dotyczących praw autorskich). /CC BY-SA (http: // creativeCommons.Org/licencje/by-sa/3.0/). Źródło: Wikimedia Commons. Materiały te są również używane w lekkich obrazach i lakierach.
W medycynie
Siarczek wapnia został uznany w badaniach medycznych jako lek w leczeniu nadciśnienia tętniczego (wysokie ciśnienie w tętnicach). Jest to choroba, która wpływa na układ sercowo -naczyniowy wielu ludzi (serce i naczynia krwionośne).
CAS jest uważany za „dawcę” H2S. Odgrywa to ważną rolę w regulacji tonu lub siły naczyń krwionośnych, więc podawanie CAS może być możliwym lekarstwem na leczenie nadciśnienia.
 Siarczek wapnia został zbadany jako możliwe lekarstwo na wysokie ciśnienie układu sercowo -naczyniowego chorych. Autor: Mohamed Hassan. Źródło: Pixabay.
Siarczek wapnia został zbadany jako możliwe lekarstwo na wysokie ciśnienie układu sercowo -naczyniowego chorych. Autor: Mohamed Hassan. Źródło: Pixabay. W uzyskiwaniu innych związków
Siark wapnia pozwala przygotować inne związki, takie jak azotan wapnia CA (NO3)2:
CAS + 2 HNO3 → Ca (nie3)2 + H2S
Zastosowano go również do uzyskania węglanu wapnia CACO3. W tym celu do węgla przesyłane jest wodne roztwór CAS2:
Cas + H2Lub + co2 → H2S + Caco3
Inne aplikacje
Siarczek wapnia jest również stosowany jako dodatek do smarów i jako środek flotacyjny w ekstrakcji minerałów.
Ryzyko
Siark wapnia może powodować podrażnienie skóry, oczu i dróg oddechowych. Musi być manipulowany środkami ostrożności i odpowiednimi narzędziami bezpieczeństwa.
Jest to bardzo toksyczny związek dla życia wodnego, więc jest niebezpieczny dla tych środowisk.
Bibliografia
- Bawełna, f. Albert i Wilkinson, Geoffrey. (1980). Zaawansowana chemia nieorganiczna. Czwarta edycja. John Wiley & Sons.
- Ołów, d.R. (redaktor). (2005). Podręcznik chemii i fizyki CRC. 85th CRC Press.
- Ropp, r.C. (2013). Grupa 16 (O, S, SE, TE) Związki Ziemi alkalicznej. Wapń siarczkowy. W encyklopedii alkalicznych związków Ziemi. Odzyskane z naukowym.com.
- Li i.F. i in. (2009). Siarczek wapnia (CAS), do dawcy siarkowodoru (H (2) s): nowy dartug przeciwnadciśnieniowy? Med Hipothes, 2009 SEP; 73 (3): 445-7. NCBI odzyskało.NLM.Nih.Gov.
- Dom j.I. i dom, k.DO. (2016). Siarka, selen i tellurium. Występują w siarce. W opisowej chemii nieorganicznej (wydanie trzecie). Odzyskane z naukowym.com.
- LUB.S. National Library of Medicine. (2019). Siark wapnia. Odzyskane z Pubchem.NCBI.NLM.Nih.Gov.
- Piwo, m. i in. (2014). Konwersja siarczku wapnia do węglanu wapnia podczas procesu odzyskiwania siarki elementarnej z odpadów gipsowych. Waste Manag, 2014 listopada; 34 (11): 2373-81. NCBI odzyskało.NLM.Nih.Gov.
- « Charakterystyka badań ilościowych, techniki, przykłady
- Właściwości krzemianu wapnia, struktura, uzyskiwanie, zastosowania »

