Maszyna Carnot
- 4894
- 277
- Pani Gilbert Stolarczyk
Co to jest maszyna Carnot?
Maszyna Carnot Jest to idealny cykliczny model, w którym ciepło jest używane do wykonywania pracy. System można rozumieć jako tłok, który porusza się wewnątrz cylindra, ściskając gaz. Wywierany przez cykl jest cykl Carnot, podany przez ojca termodynamiki, francuskiego fizyka i inżyniera Nicolasa Leonarda Sadi Carnota.
Carnot stwierdził ten cykl na początku XIX wieku. Maszyna jest poddawana czterem wariantom stanu, naprzemiennie, takim jak stała temperatura i ciśnienie, w których wykazano zmianę objętości podczas ściskającego i rozszerzającego gaz gazu.
Formuły
Według Carnota poddanie idealnej maszyny do zmian temperatury i ciśnienia możliwe jest zmaksymalizacja uzyskanej wydajności.
Cykl Carnota musi być analizowany osobno w każdej z czterech faz: ekspansja izotermiczna, rozszerzanie adiabatyczne, kompresja izotermiczna i kompresja adiabatyczna.
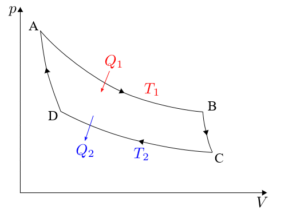
Formuły związane z każdą z faz cyklu wywieranego na maszynę Carnot zostaną szczegółowo opisane poniżej.
Ekspansja izotermiczna (A → B)
Połączenia tej fazy są następujące:
- Objętość gazu: Przechodzi od minimalnej objętości do średniej objętości.
- Temperatura maszyny: stała temperatura T1, wysoka wartość (T1> T2).
- Ciśnienie maszyny: Zejdź z P1 do P2.
Proces izotermiczny oznacza, że temperatura T1 nie różni się w tej fazie. Przenoszenie ciepła indukuje ekspansję gazu, co indukuje ruch na tłoku i wytwarza prace mechaniczne.
Podczas ekspansji gaz stanowi pewną tendencję do chłodzenia. Jednak pochłania ciepło emitowane przez źródło temperatury i podczas jego rozszerzenia utrzymuje stałą temperaturę.
Może ci służyć: jaka jest prędkość liniowa? (Z rozwiązanymi ćwiczeniami)Ponieważ temperatura pozostaje stała podczas tego procesu, energia wewnętrzna gazu nie zmienia się, a całe ciepło pochłaniane przez gaz jest skutecznie przekształcane w pracę. Więc:
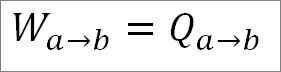
Z drugiej strony, na końcu tej fazy cyklu można również uzyskać wartość ciśnienia za pomocą równania gazu idealnego. W ten sposób masz następujące czynności:
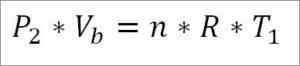
W tym wyrażeniu:
- P2: Presja na końcu fazy.
- VB: Tom w punkcie B.
- N: Liczba moli gazu.
- Odp.: Uniwersalna stała gazów idealnych. R = 0,082 (atm*litr)/(mole*k).
- T1: Absolutna temperatura początkowa, stopnie Kelvin.
Rozszerzenie adiabatyczne (B → C)
Podczas tej fazy procesu ekspansja gazu jest przeprowadzana bez potrzeby wymiany ciepła. W ten sposób przesłanki są szczegółowo opisane:
- Objętość gazu: Przechodzi od średniej objętości do maksymalnej objętości.
- Temperatura maszyny: Zejdź z T1 do T2.
- Ciśnienie maszyny: stałe ciśnienie p2.
Proces adiabatyczny oznacza, że ciśnienie P2 nie różni się w tej fazie. Temperatura maleje, a gaz nadal się rozwija, aż osiągnie maksymalną liczbę objętości; to znaczy tłok dociera do góry.
W takim przypadku wykonane prace pochodzi z energii wewnętrznej gazu, a jego wartość jest ujemna, ponieważ energia zmniejsza się podczas tego procesu.
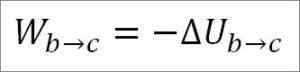
Zakładając, że jest to gaz idealny, teoria utrzymuje się, że cząsteczki gazowe mają tylko energię kinetyczną. Zgodnie z zasadami termodynamiki można to wywnioskować w następującym wzorze:
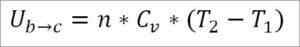
W tym formule:
- ∆UB → C: Wewnętrzna zmiana energii idealnego gazu między punktami B i C.
- N: Liczba moli gazu.
- CV: Gazowa molowa pojemność cieplna.
- T1: Absolutna temperatura początkowa, stopnie Kelvin.
- T2: Absolutna temperatura końcowa, stopnie Kelvin.
Kompresja izotermiczna (C → D)
W tej fazie rozpoczyna się kompresja gazu; Oznacza to, że tłok jest mobilizowany do cylindra, z którym gaz kurczy się.
Warunki związane z tym procesem są szczegółowe poniżej:
- Objętość gazu: Przechodzi od maksymalnej objętości do objętości pośredniej.
- Temperatura maszyny: stała temperatura T2, zmniejszona wartość (T2 < T1).
- Ciśnienie maszyny: Wzrost z P2 do P1.
Tutaj wzrasta ciśnienie na gaz, więc zaczyna ściskać. Jednak temperatura pozostaje stała, a zatem wewnętrzna zmiana energii gazu wynosi zero.
Analog do ekspansji izotermicznej, wykonana praca jest równa ciepło systemu. Więc:
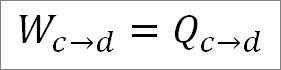
Możliwe jest również znalezienie ciśnienia w tym momencie za pomocą równania gazowego idealnego.
Kompresja adiabatyczna (d → a)
Jest to ostatnia faza procesu, w której system powraca do swoich początkowych warunków. Aby to zrobić, rozważane są następujące warunki:
- Objętość gazu: Przechodzi od objętości pośredniej do minimalnej objętości.
- Temperatura maszyny: Wzrost z T2 do T1.
- Ciśnienie maszyny: stałe ciśnienie p1.
Źródło ciepła włączone do układu w poprzedniej fazie jest usuwane, aby gaz idealny podniosła swoją temperaturę w międzyczasie ciśnienie.
Gaz powraca do początkowych warunków temperatury (T1) i przy jego objętości (minimum). Po raz kolejny wykonana praca pochodzi z wewnętrznej energii gazu, więc musisz:
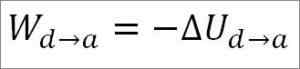
Podobnie jak w przypadku ekspansji adiabatycznej, możliwe jest uzyskanie zmiany energii gazowej poprzez następujące wyrażenie matematyczne:
Może ci służyć: fluor wapnia (CAF2): struktura, właściwości, zastosowania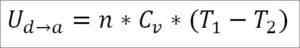
Jak działa maszyna Carnot?
Maszyna Carnot działa jako silnik, w którym wydajność jest maksymalizowana przez zmienność procesów izotermicznych i adiabatycznych, na przemian faz ekspansji i zrozumienia idealnego gazu.
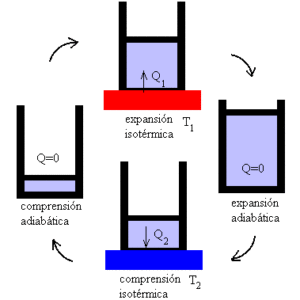
Mechanizm można zrozumieć jako idealne urządzenie, które wykonuje zadanie poddawane zmianom cieplnym, biorąc pod uwagę istnienie dwóch reflektorów temperaturowych.
Na pierwszym skupieniu system jest narażony na temperaturę T1. Jest to wysoka temperatura, która poddaje system obciążający i wytwarza rozszerzenie gazu.
Z kolei przekłada się to na wykonanie pracy mechanicznej, która umożliwia mobilizację tłoka z cylindra i którego limit jest możliwy tylko dzięki rozszerzeniu adiabatyczne.
Następnie pojawia się drugi skupienie, w którym system jest narażony na temperaturę T2, mniejszą niż T1; to znaczy mechanizm podlega chłodzeniu.
To indukuje ekstrakcję ciepła i kruszenie gazu, które osiąga początkową objętość po kompresji adiabatycznej.
Aplikacje
Maszyna Carnot była szeroko stosowana dzięki jej wkładowi w zrozumienie najważniejszych aspektów termodynamiki.
Ten model pozwala jasno zrozumieć zmiany gazów idealnych podlegających zmianom temperatury i ciśnienia, co jest metodą referencyjną przy projektowaniu prawdziwych silników.