Gilbert Newton Lewis
- 1406
- 126
- Prokul Woliński
 Gilbert Newton Lewis
Gilbert Newton Lewis Gilbert Newton Lewis (1875–1946) był jednym z najważniejszych amerykańskich naukowców XX wieku. Jego prace stworzyły rewolucję strukturalną w badaniach chemicznych, dzięki wielokrotnemu wkładowi przez całe życie w rozwoju nauki.
Wśród wkładu tego fizykochemicznego wyróżnia się formuły, która nosi jego imię, z którym pary elektronów są reprezentowane graficznie. Prace badawcze Lewisa były bardzo szerokie, chociaż jego sława była zasadniczo spowodowana teorią wiązań chemicznych i definicji kwasu kwasowego w 1923 r.
Lewis miał wielki wpływ na świat naukowy i akademicki Stanów Zjednoczonych, szczególnie na Harvard University, gdzie utworzono i podyktowano przewodniczącego. Jego praca dla armii amerykańskiej podczas I wojny światowej przyniosłem mu największe uznanie i najwyższe wyróżnienia.
Został utworzony na uniwersytetach Nebraski, Harvardu, Lipsku i Gontinga w Niemczech. Pracował w Massachusetts Institute (MIT), na Uniwersytecie Harvard i na University of California, gdzie zmarł w pracy.
Przez całe życie otrzymywał niezliczone uznanie i nagrody, w tym kilka honorowych doktoratów z Chicago, Madrytu, Liverpoolu, Wisconsin i Pensylwanii. Był honorowym członkiem kilku instytucji naukowych w Anglii, Indiach, Szwecji, Danii i Stanach Zjednoczonych.
Biografia
Poród i wczesne lata
Gilbert Newton Lewis urodził się w Weymouth, Massachusetts, 23 października 1875 r. Jego rodzicami byli Frank Wesley Lewis i Mary Burr White Lewis. We wczesnych latach otrzymał nauki we własnym domu, a o 10 lat wszedł do szkoły publicznej, gdzie ukończył studia w 1889 roku.
W 1884 roku Lewis musiał osiedlić się ze swoją rodziną w Lincoln w stanie Nebraska. W wieku 13 lat został przyjęty do liceum University of Nebraska.
Może ci służyć: wodorot beryl (beh2)Studia
Kiedy ukończył studia, kontynuował studia uniwersyteckie przez dwa lata, a następnie zapisał się na Uniwersytet Harvarda w 1893 roku.
Początkowo był zainteresowany gospodarką, ale w końcu wybrał fizykę i chemię. Gilbert uzyskał tytuł w chemii w 1896 roku i przez rok uczył w Phillips Academy, prywatnej szkole dla Andover.
Wrócił na Harvard, aby wykonać pracę podyplomową i uzyskał tytuł magistra w 1898 r Elektron i cząsteczka. Rok później doktorat i jego teza nosiła tytuł Niektóre relacje elektrochemiczne i termochemiczne amalgamat cynku i kadmu".
Na Harvardzie przez rok był instruktorem, a następnie udał się do Europy ze stypendium. Studiował z wielkimi fizykochemicznymi tamtejmi czasami.
W 1899 r. Pojechał do Niemiec, aby studiować z Wilhelmem Ostwaldem Lipskiem, a następnie z Walterem Nernstem na University of Gontinga; Potem pracował dla rządu filipińskiego.
Praca akademicka i udział w wojnie
W latach 1999–1906 wydał przewodniczącego chemii na Harvard University, a następnie zatrudniony przez Massachusetts Institute of Technology, gdzie był w latach 1907–1912.
Później został profesorem chemii fizycznej na University of California (Berkeley), gdzie uzyskał stopień dziekana School of Chemistry.
W 1908 roku opublikował swój pierwszy artykuł na temat teorii względności w równoległości z Albertem Einsteinem. W tym stwarza, że istnieje związek między Masą energii, ale w kierunku innego niż ten zastosowany przez Einsteina.
21 czerwca 1912 roku Lewis poślubił Mary Fanckley Sheldon, z którą miał troje dzieci: Margery S. Lewis, Edward S. Lewis i Richard Newton Lewis.
Może ci służyć: kwas giberéliczny: charakterystyka, synteza, funkcjeJego prace w Kalifornii zostały przerwane przez wybuch I wojny światowej. W 1917 r.
Dostawa i zdolności pracy Lewisa pozwoliły armii. Pod koniec wojny został przyznany za swoje usługi z najwyższymi zaszczytami.
Śmierć w laboratorium
Gilbert n. Lewis zmarł w wieku 70 lat na atak serca, kiedy pracował w swoim laboratorium na University of Berkeley, 23 marca 1946 r.
Być może ze względu na introwertyczną osobowość ten wybitny naukowiec nigdy nie otrzymał Nagrody Nobla. Niemal pod koniec swojej kariery udało mu się udowodnić, że fosforescencja cząsteczek organicznych jest regulowana przez podekscytowany stan trypletu, nawet obliczając jego właściwości magnetyczne.
Wkład w naukę
Niektóre z najważniejszych wkładów Gilberta Newtona Lewisa w naukę są następujące:
Struktury Lewisa
Są to kilka metod, które służą do reprezentowania struktury cząsteczki. W tych symboli elementów reprezentują atomy, podczas gdy punkty reprezentują otaczające je elektrony. Przykładem tego jest reprezentacja wodoru, helu i węgla:
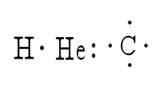
Lewis jako pierwszy zaproponował ideę, że atomy mogą pozostać zjednoczone poprzez porównanie par elektronów; Dlatego stworzył symbolikę struktur.
Teoria szerokiego ogniwa zaproponowana przez Lewisa służyła grupie w jednym koncepcji wszystkie rodzaje linków chemicznych. W ten sposób wykazano związki między substancjami jonowymi, molekularnymi, kowalencyjnymi i metalowymi. Do tego czasu te elementy nie miały żadnego połączenia koncepcyjnego.
Może ci służyć: rodzaj linku 02Wiązanie kowalencyjne
Konceptualizowano wiązanie kowalencyjne, które tworzy między dwoma atomami, gdy łączą się, aby osiągnąć stabilny oket i dzielą elektrony ostatniego poziomu, z wyjątkiem wodoru, który udaje się osiągnąć stabilność poprzez posiadanie 2 elektronów.
Teoria oktetów
Lewis stwierdził w 1916 roku. Stwierdza to, że jony należące do elementów systemu okresowego mają tendencję do kompetencji z wieloma 8 elektronów ich najnowszych poziomów energii. To pozwala im uzyskać bardzo stabilną konfigurację.
Foton
W 1926 r. Był twórcą terminu, aby wyznaczyć najmniejszą jednostkę energii świetlnej. Ta cząsteczka energii przesyła wszystkie istniejące formy promieniowania elektromagnetycznego (x -kas, podczerwień, gamma, ultrafiolet, mikrofale, fale radiowe itp.).
Przyciąganie chemiczne i walencja
Wraz ze swoim kolegą chemicznym Irwing Langmirem opracował teorię przyciągania i walencji chemicznej, znaną jako teoria Langmuir-Lewis. W tym celu opierało się to na strukturze atomowej substancji.
Ciężka woda
Lewis był także pierwszym naukowcem, który badał i produkował ciężką wodę (deuter) w najczystszej postaci. Jako pierwszy zastosował zasady termodynamiki w badaniu problemów chemicznych.
Teoria rozwiązania
Podobnie Lewis jest rozpoznawany na temat teorii rozwiązań; to znaczy jednorodne mieszaniny uzyskane z interpozycji atomów, cząsteczek lub jonów obecnych w dwóch lub więcej substancjach. Substancje te nazywane składnikami interweniując w proporcjach, które się różnią.

