Enancjomery
- 4295
- 719
- Maksymilian Kępa
Wyjaśniamy, jakie enancjomery i chiralność, ich właściwości, nomenklatura i kilka przykładów
 Te dwa związki są enancjomerami, ponieważ są one tworzone przez te same atomy, zjednoczone w ten sam sposób
Te dwa związki są enancjomerami, ponieważ są one tworzone przez te same atomy, zjednoczone w ten sam sposób Jakie są enancjomery?
Enancjomery Są to pary związków, które są niezmiennymi lustrzanymi obrazami. Te pary związków są szczególnym rodzajem izomerów, to znaczy są różnymi związkami, które mają ten sam wzór molekularny.
Istnieją wśród różnych rodzajów izomerów stereoizomerów, w których wszystkie atomy są zjednoczone w tej samej kolejności i z tym samym typem linków, ale mają różne orientacje w przestrzeni (stereo oznacza przestrzeń).
W stereoizomerach znajdujemy enancjomery, których główną cechą są ze sobą obrazy lustrzane.
Enancjomery są bardzo powszechne z natury. W rzeczywistości prawie wszystkie związki organiczne obecne w komórkach wszystkich żywych istot są jednym z dwóch możliwych enancjomerów.
Na przykład wszystkie aminokwasy, które są częścią naturalnych białek, odpowiadają enancjomerowi L odpowiedniego aminokwasu (drugi izomer identyfikuje się z literą D).
Z drugiej strony, aktywne składniki zdecydowanej większości leków istnieją również jako pary enancjomerów, z których tylko jedna jest skuteczna. Trudność w oddzielaniu enancjomerów od siebie oznacza, że leki zawierające tylko użyteczny izomer są bardzo drogie.
Enancjomery i chiralność
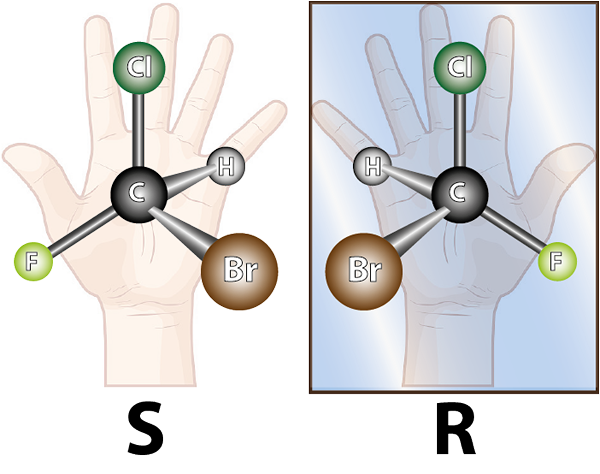
Enancjomery powstają przez cząsteczki chiralne. Chiralność jest właściwością, że nie można się nakładać z lustrzanym obrazem. Słowo Chiral pochodzi z greckiego terminu, Kheir co oznacza rękę, pamiętając fakt, że ręce są również obrazami i nie mogą się nakładać.
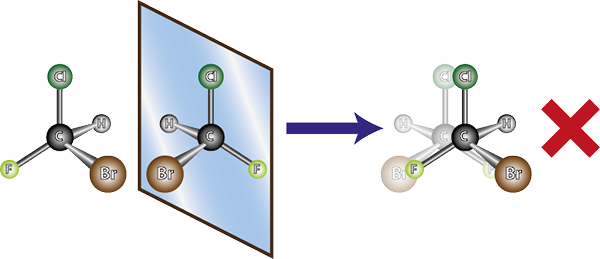 Cząsteczka lewej jest chiralna, ponieważ podczas porównywania jej z lustrzanym obrazem można zauważyć, że nie nakładają się. Innymi słowy, nie ma sposobu na obracanie się lub obrócenie w taki sposób, aby wszystkie atomy się ze sobą pokrywają
Cząsteczka lewej jest chiralna, ponieważ podczas porównywania jej z lustrzanym obrazem można zauważyć, że nie nakładają się. Innymi słowy, nie ma sposobu na obracanie się lub obrócenie w taki sposób, aby wszystkie atomy się ze sobą pokrywają W związku z powyższym można wywnioskować, że dla każdej chiralnej cząsteczki musi istnieć inna chiralna cząsteczka, która nie jest jej nakładającą się obrazem lustrzanym, czyli jej enancjomer. Innymi słowy, ilekroć mówi się, że cząsteczka.
Może ci służyć: neodym: struktura, właściwości, użyciaCentra chiralne
Wiele związków chiralnych ma jeden lub więcej asymetrycznych centrów odpowiedzialnych za chiralność cząsteczki. Są one nazywane centrami chiralnym, a w wielu związkach organicznych składają się z atomów węgla, które są powiązane z 4 atomami lub grupami różnych atomów.
Szczególna postać jako cztery grupy są rozmieszczone wokół asymetrycznego węgla. Obecność pojedynczego ośrodka Quiral zapewnia, że cząsteczka jest chiralna, ale jeśli jest więcej niż jedna, może być chiralna, jak może nie.
Właściwości enontiomera
Większość właściwości fizycznych i chemicznych jest identyczna
Jak prawa ręka i lewa ręka, enancjomery przychodzą tylko parami. Te związki są praktycznie identyczne z sobą. W rzeczywistości większość jego właściwości fizycznych i chemicznych, takich jak punkt fuzji, wrzenia, ciśnienie pary i rozpuszczalność w niektórych rozpuszczalnikach, jest identyczna.
Aktywność optyczna
Wszystkie związki chiralne mają unikalną właściwość, która odróżnia ich od tych, którzy nie są: mają zdolność obracania płaszczyzny światła spolaryzowanego. Ta właściwość nazywa się Aktywność optyczna, I jest to jedna z niewielu właściwości, które odróżniają chiralny związek od jego enancjomeru.
Ten ostatni wynika z faktu, że spolaryzowana płaszczyzna światła można obrócić w jednym z dwóch kierunków, albo w kierunku igieł zegara (zwanych dexstrogyr i reprezentowaną z symbolem +), albo na igłach zegara (Levógiro, reprezentowana z The the the the Reprezentowana z symbol -).
Jeśli związek quiralny obraca spolaryzowaną płaszczyznę światła w jednym kierunku, jego enancjomer obróci go w przeciwnym kierunku.
-
Przykład
Roztwór d-glukozy obraca spolaryzowaną płaszczyznę światła w kierunku igieł zegara (po prawej stronie, jest to dekstrogyral), podczas gdy roztwór L-glikoza sprawia, że obraca się w przeciwnym kierunku.
Może ci służyć: Erlenmeyer Folask: Charakterystyka, zastosowania, metody użytkowaniaRóżnicowa reaktywność
Kolejną właściwością, która pozwala odróżnić jedno enantión od drugiego, jest jej reaktywność wobec innych związków chiralnych.
Różnicową reaktywność można porównać do sposobu, w jaki rękawica wygląda tylko z jednej strony, ale nie drugą, lub jako prawy but dobrze pasuje do prawej stopy, ale nie w lewo.
Ważną konsekwencją reaktywności różnicowej jest różne skutki, które mogą powodować dwa enancjomery niektórych leków. Różnice te mogą być nieszkodliwe, ale mogą być również bardzo niebezpieczne.
-
Przykłady
- Z dwóch enantimerów aspartamu (który jest sztucznym słodzikiem), jeden jest słodki, a drugi nie ma smaku.
- Tylko enancjomer omeprazolu jest skuteczny jako obrońca żołądka, podczas gdy drugi nie wytwarza żadnego efektu.
- D-penicylamina jest lekiem przeciwko reumatoidalnym zapaleniem stawów, podczas gdy jej enancjomer, L-penicylamina jest niebezpieczną trucizną.
Wchłanianie różnicowe
Enancjomery różnią się również w sposobie wchłaniania żywic lub ciał stałych, które są również chiralami. Mieszaninę enancjomerów można oddzielić, jeśli zostanie przekazana przez kolumnę o separacji chiralnej, ponieważ jeden z dwóch enancjomerów zostanie pochłonięty silniej niż drugi.
Nomenklatura enancjomerów
Istnieje kilka metod identyfikacji jednego lub drugiego enancjomeru, ale najczęściej używanym jest system Cahn-Ingold-Prelog (CIP). Składa się to z następujących kroków:
- Poziom hierarchii jest przypisany do czterech grup dołączonych do każdego centrum chiralnego. Priorytet grup jest przypisywany zgodnie z liczbą atomową atomu bezpośrednio powiązanego z centrum Quiral. Jeśli istnieją dwa równe atomy, liczby atomowe atomów, które są powiązane z pierwszym, są dodawane w celu dodania liczb atomowych.
- Kierunek, w którym trzy grupy priorytetowe są podróżowane, gdy ustalone są punkty najniższych punktów priorytetu.
- Jeśli kierunek trasy znajduje się w kierunku dłoni zegara, przypisana jest konfiguracja R, W przeciwnym razie przypisana jest konfiguracja S.
Przykład
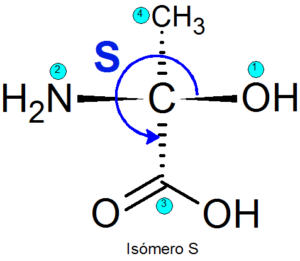
Przykłady enancjomerów
D-gliceraldehyd i L-gliceraldehyd
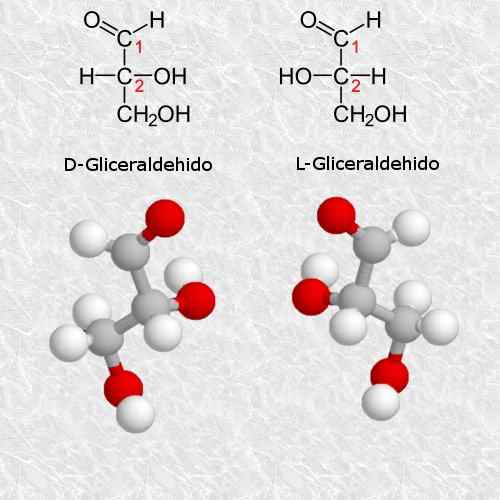
Gliceraldehyd jest najprostszym i najbardziej małym quiralnym węglowodanem, który istnieje i jest bardzo ważny dla chemii i biologii.
Zgodnie z zasadami systemu Cahn-Ingold-Prelog izomer D odpowiada izomerowi (R), a izomer L odpowiada (s) (s) (s).
D-Alanina i L-Alanina
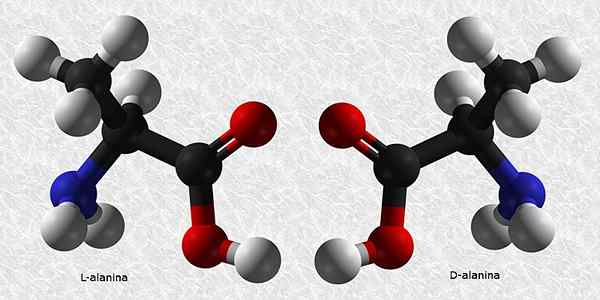
Alanina jest jednym z niezbędnych aminokwasów do budowy białek. Podobnie jak prawie wszystkie aminokwasy, ma chiralny węgiel, więc ma dwa enancjomery:
Z tych dwóch L-Alanina jest najczęstsza i obecna we wszystkich żywych istotach, podczas gdy D-Alanina jest obecna tylko w niektórych ścianach komórkowych bakteryjnych.
Kwas D-tartaryczny i L-tartarowy
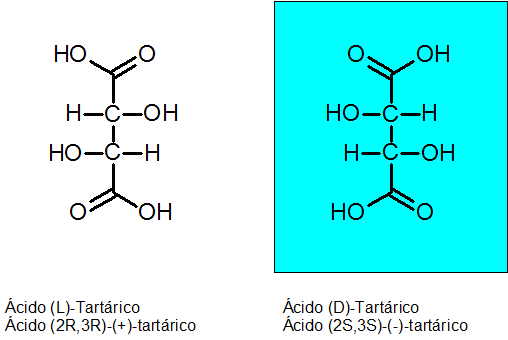
Chiralność została odkryta przez Louisa Pasteura w 1848 roku. Ten związek ma 2 asymetryczne węgle i mogą istnieć jako dwa enancjomery plus trzeci izomer nazywany Meso Compound.
Absolutna konfiguracja dwóch chiralnych węgli to r dla enancjonio levógiro i s dla enantiomu dextrogyan.
2-butanol
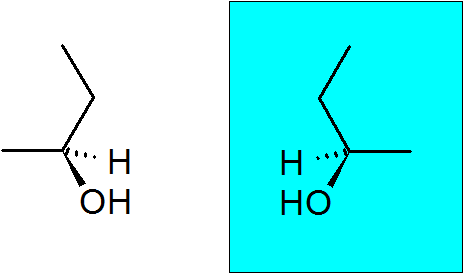
Ten alkohol ma również quiralny węgiel, który sprawia, że ten związek ma dwa enancjomery.
Bromokloroetan
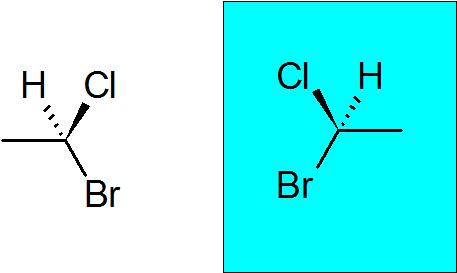
Jest to bardzo prosty związek chiralny z tylko dwoma węglemi. Quiralny węgiel dołączył do bromu, chloru, metylu i wodoru.
Bibliografia
- Chiralność (chemia). (18 marca 2021 r.) Na Wikipedii.com
- Carey, f. DO. (2008). Chemia organiczna. Boston: szkolnictwo wyższe McGraw-Hill.
- Smith, m., Marzec, J., & March, J. (2001). Zaawansowana chemia organiczna marcowego: reakcje, mechanizmy i pasek. Nowy Jork: Wiley.
- M.H. Hyun (2012). 8.13 Separacje i analiza chromatograficzna: Chiralne chiralne fazy stacjonarne oparte na koronie koronnej. Redaktor: Erick M. Carreira, Hisashi Yamamoto. Zrozumienie chiralności. Elsevier. Strony 263-285. ISBN 9780080951683,
- Nguyen, L. DO., On, h., & Pham-Huy, c. (2006). Chiralne leki: przegląd. International Journal of Biomedical Science: IJBS, 2(2), 85-100.

