Struktura chemiczna kwasu borowego, właściwości, przygotowanie, zastosowania

- 1613
- 45
- Gabriela Łuczak
On kwas borowy Jest to związek nieorganiczny, którego wzorem chemicznym jest h3Bo3. Składa się z białej lub bezbarwnej stałej. Jest to słaby kwas, który wytwarza roztwór wodny, w zależności od jego stężenia, pH od 3,8 do 4,8. Jest mało rozpuszczalny w zimnej i umiarkowanie rozpuszczalnej gorącej wodzie.
Kwas borowy został odkryty w 1702 roku przez Wilhelma Man.
 Stała próbka kwasu borowego na szklance zegara. Źródło: Walkerma przez Wikipedia.
Stała próbka kwasu borowego na szklance zegara. Źródło: Walkerma przez Wikipedia. Jednak wskazano również, że Boerg przygotował kwas borowy, dodając wodę do boraksu i podgrzewając roztwór, aby go odparować, pozostawiając w ten sposób osad kryształy kwasu krialnego.
Kwas ten jest bardzo przydatnym związkiem, który ma liczne zastosowania w przemyśle i medycynie, również stosowane jako środki owadobójcze, zachowanie drewna, opóźniający ogień i jest składnikiem roztworu tłumienia pH.
[TOC]
Struktura chemiczna
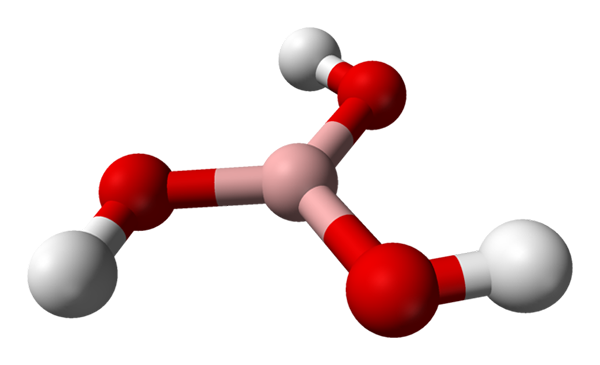 Cząsteczka kwasu borowego reprezentowana przez model kulki i słupków. Źródło: Benjah-BMM27 [domena publiczna]
Cząsteczka kwasu borowego reprezentowana przez model kulki i słupków. Źródło: Benjah-BMM27 [domena publiczna] Na lepszym obrazie mamy samą cząsteczkę H3Bo3. Należy zauważyć, że atomy wodoru, reprezentowane przez białe kule, nie są powiązane z środkowym atomem boru, jak można sugerować wzór chemiczny; ale raczej, do atomów tlenu, reprezentowane przez czerwone kule.
Zatem wygodniejsza formuła, choć mniej używana, do kwasu borowego jest B (OH)3, wskazując, że ich kwasowość wynika z jonów H+ Wyzwoleni z ich grup OH. Molecula B (OH)3 Ma płaską geometrię trygonalną, z atomem boru z hybrydyzacją chemiczną sp2.
B (OH)3 Jest to kowalencyjna wysoka cząsteczka, ponieważ różnica w elektroonywności między atomem boru a tlenem nie jest zbyt duża; Tak więc linki B-O są w istocie kowalencyjne. Zauważ, że struktura tej cząsteczki przypomina strukturę spinnera. Czy mogę włączyć twoją własną oś w ten sam sposób?
Kryształy
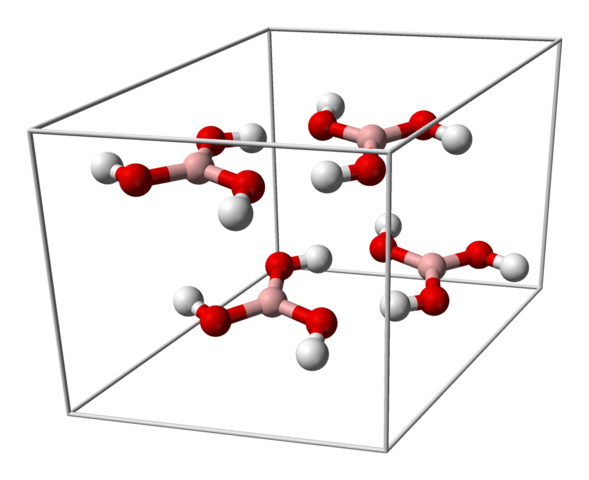 Jednolita komórka dla kryształu H3BO3. Źródło: Benjah-BMM27 [domena publiczna]
Jednolita komórka dla kryształu H3BO3. Źródło: Benjah-BMM27 [domena publiczna] Górny obraz pokazuje jednolitową komórkę odpowiadającą trójkołowej strukturze krystalicznej kwasu borowego, który w określonych warunkach syntezy może przyjąć zwartą strukturę sześciokątną. Zauważ, że istnieją cztery cząsteczki na jednolitą komórkę, które są uporządkowane w dwóch warstwach, A i B, naprzemiennie (nie są one nałożone na siebie).
Z powodu symetrii i wskazówek łączy B-OH można założyć, że B (OH)3 Jest apolarna; Jednak istnienie międzycząsteczkowych mostów wodoru zmienia historię. Każda cząsteczka B (OH)3 Aby dać lub otrzymać trzy z tych mostów, z sumą sześciu interakcji dipol-dipolo, takich jak te obserwowane na poniższym obrazku:
Może ci służyć: terpenos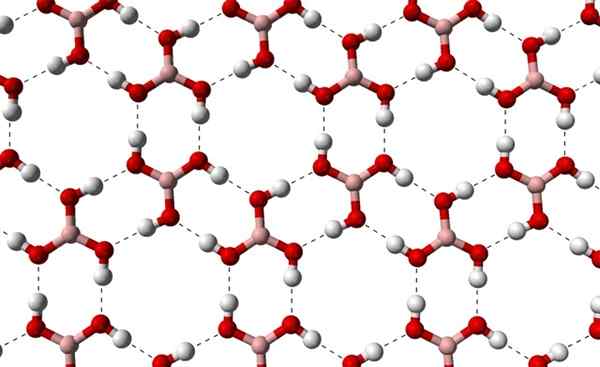 Krystaliczne warstwy H3BO3 obserwowane z wyższej osi. Źródło: Benjah-BMM27 [domena publiczna]
Krystaliczne warstwy H3BO3 obserwowane z wyższej osi. Źródło: Benjah-BMM27 [domena publiczna] Należy zauważyć, że te mosty wodorowe są interakcjami kierunkowymi, które rządzą kryształami kwasu borowego i ustalają wzorce aspektów ozdobnych; Pierścienie wewnętrzne być może z wystarczającą przestrzenią, aby zamknąć zanieczyszczenia, które nie są w defektach krystalicznych.
Te mosty wodorowe, pomimo niskiej masy cząsteczkowej B (OH)3, Utrzymują szklane spójne, że potrzebuje temperatury 171 ° C, aby się stopić. Nie wiadomo, jakie efekty miałyby wysokie ciśnienie (w kolejności GPA) na warstwy molekularne B (OH)3.
Nieruchomości
Nazwy
IUPAC: kwas borowy i trihydrooksydobor. Inne nazwy: kwas ortoboryczny, kwas kraksowy, sassolit, borofax i trihydroksyborano.
Masa cząsteczkowa
61,83 g/mol
Wygląd fizyczny
Krystaliczne, bezbarwne i przezroczyste białe ciało stałe. Osiąga się również jako granulki lub w postaci białego pyłu. Nieco niezadowolone do dotknięcia.
Zapach
Toaleta
Smak
Nieco gorzki
Temperatura topnienia
170,9 ºC
Punkt wrzenia
300 ° C
Rozpuszczalność wody
Umiarkowanie rozpuszczalny w zimnej i rozpuszczalnej wodzie w gorącej wodzie:
2,52 g/100 ml (0 ºC)
27,50 g/100 ml (100 ºC)
Kwas borowy jest częściowo rozpuszczalny w wodzie i ma tendencję do zapadania się. Ta rozpuszczalność ma tendencję do wzrostu w obecności kwasów, takich jak chlorowodor, cytryn.
Rozpuszczalność w innych rozpuszczalnikach
-Glicerol: 17,5 % w 25 ° C
-Glikol etylenowy: 18,5 % w 25 ° C
-Aceton: 0,6 % w 25 ° C
-Octan etylu: 1,5 % w 25 ° C
-Metanol: 172 g/l 25 ºC
-Etanol: 94,4 g/l 25 ºC
Współczynnik podziału oktanol/wodę
Log p = -0,29
Kwasowość (PKA)
9.24. 12.4. 13.3. Są to trzy stałe ich odpowiednich dysocjacji w celu uwolnienia H+ W wodzie.
Ph
3,8 - 4,8 (3,3 % w roztworze wodnym)
5.1 (0,1 trzonowiec)
Ciśnienie pary
1,6 · 10-6 MMHG
Stabilność
Stabilny w wodzie
Rozkład
Rozkłada się, gdy ogrzewa się powyżej 100 ° C, tworząc bezwodnik borowy i wodę.
Reaktywność
Kwas borowy tworzy rozpuszczalne sole z monowalentnymi kationami, na przykład: na2B4ALBO7.10h2Lub i nierozpuszczalne sole z białkowymi kationami, kabiną4ALBO7.6h2ALBO.
W roztworze wodnym wytwarza roztwór kwasowy, myśląc, że ta właściwość była spowodowana odejmowaniem grup OH- z wody. Kwas borowy jest kwalifikowany jako słaby kwas typu Lewisa.
Kwas borowy reaguje z glicerolem i mannitolem, zwiększając kwasowość środowiska wodnego. PKA jest modyfikowana z 9,2 do 5, ze względu na utworzenie boro-manitolu Quelato [BC6H8ALBO2(OH)2]-, który uwalnia h+.
Przygotowanie
Kwas borowy jest w stanie swobodnym w emanacji wulkanicznych w regionach takich jak Toskania Włoch, Wyspy Lipari i w stanie Nevada, USA. Występuje również w minerałach, takich jak Boraks, Boracita, Ulexita i Colemanita.
Może ci służyć: halogenyKwas borowy jest głównie wytwarzany przez reakcję minerału boraksu (tetraboracie sodu sodu) z kwasami mineralnymi, takimi jak kwas solny, kwas siarkowy itp.
Na2B4ALBO9· 10H2O +hcl => 4 h3Bo3 + 2 NaCl +5 H2ALBO
Jest również przygotowywany przez hydrolizę Boro i Diborano Trihaluro.
Kwas borowy jest przygotowywany z Collemanite (CA2B6ALBOjedenaście· 6 godzin2ALBO). Procedura polega na leczeniu mineralnym kwasem siarkowym w celu rozpuszczenia związków boru.
Następnie roztwór, w którym występuje kwas borowy fragmentów rozdzielonych, jest oddzielony. Roztwór wodoru siarczku jest traktowany w celu wytrącania zanieczyszczeń arsenu i żelaza. Supernatant jest chłodzony w celu wytworzenia osadu kwasu borowego i oddzielić go od zawiesiny.
Aplikacje
W przemyśle
Kwas borowy jest stosowany w opracowaniu włókna szklanego. Przyczyniając się do zmniejszenia temperatury topnienia, zwiększa wytrzymałość i wydajność włókna szklanego: materiał używany do wzmocnienia plastiku stosowanego w naczyniach, rurach przemysłowych i płytach obwodów komputerowych.
Kwas borowy bierze udział w produkcji szklanki borozolizowanej, co pozwala uzyskać szklane szkło, użyteczne w kuchni domowej, w szklanym materiale laboratoriów, rur fluorescencyjnych, ekranach światłowodowych, ekranach LCD itp.
Jest stosowany w przemyśle metalurgicznym do stwardnienia i leczenia stopów stalowych, a także faworyzowania metalowej podszewki materiałów.
Jest stosowany jako składnik chemiczny w szczelinowaniu hydraulicznym (szczelinowanie): metoda stosowana w ekstrakcji oleju i gazu. Kwas borowy działa jak opóźnienie ogniowe w materiałach celulozowych, tworzyw sztucznych i tekstyliach, które są impregnowane kwasem borowym w celu zwiększenia odporności na ogień.
W medycynie
Kwas borowy jest stosowany w myciu oczu. Kapsułki żelatyny kwasu borowego stosuje się do leczenia infekcji grzybiczych, zwłaszcza Candida albicans. Został również stosowany w leczeniu trądziku.
Kwas borowy jest posypany skarpetami, aby zapobiec infekcjom stóp, takimi jak stopa sportowca. Podobnie roztwory zawierające kwas borowy są stosowane w leczeniu zewnętrznego zapalenia ucha u ludzi, a także u zwierząt.
Kwas borowy dodaje się w butelkach stosowanych do pobierania moczu, co zapobiega zanieczyszczeniu bakteryjnym przed badaniem w laboratoriach diagnostycznych.
Może ci służyć: kwas indolalny: struktura, właściwości, uzyskiwanie, zastosowaniaŚrodek owadobójczy
Kwas borowy stosuje się w kontroli proliferacji owadów, takich jak karaluchy, termity, mrówki itp. Karaluchy nie zabijają natychmiast, ponieważ najpierw wpływa na jego układ trawienny i nerwowy, oprócz niszczenia egzoszkieletu.
Kwas borowy powoli wywiera swoje działanie, pozwalając owadom, które połknęły go na kontakt z innymi owadami, rozprzestrzeniając w ten sposób zatrucie.
Ochrona
Kwas borowy służy do zapobiegania atakowi drewna przez grzyby i owadów, stosowane w tym celu w połączeniu z glikolem etylenowym. To leczenie jest również skuteczne w kontroli mułu i glonów.
PH Absorbber
Kwas borowy i jego sprzężona zasada tworzą system tłumienia PKA = 9,24, który wskazuje, że ten amortyzator ma największą skuteczność w alkalicznym pH, które nie są zwykle w żywych istotach. Jednak amortyzator wstrząsu Borato jest stosowany w regulacji pH w basenach.
Reaktor nuklearny
Kwas borowy ma zdolność do przechwytywania neutronów termicznych, co zmniejsza możliwość niekontrolującego rozszczepienia jądrowego, które może wytwarzać wypadki jądrowe.
Rolnictwo
Boro jest niezbędnym elementem wzrostu roślin, który wywołał użycie kwasu borowego do udziału elementu. Jednak w nadmiarze kwasu borowego może uszkodzić rośliny, zwłaszcza owoce cytrusowe.
Przeciwwskazania
Zastosowanie kwasu borowego na wyczerpanej skórze, rany lub spalanie, który pozwala na wchłanianie tego samego. Jest to toksyczny związek wewnątrz ciała, aw niektórych przypadkach może powodować omdlenie, napady, skurcze, tiki twarzy i niedociśnienie tętnicze.
Należy skonsultować się z lekarzem w sprawie stosowania kapsułek pochwy kwasu borowego u kobiet w ciąży, ponieważ wskazano, że deformacje płodu i zmniejszenie masy ciała dziecka po urodzeniu mogą wytwarzać po urodzeniu.
Umieszczenie kwasu borowego, stosowanego jako owadobójczy, w miejscach dostępnych dla dzieci, ponieważ dzieci mają większą podatność na toksyczne działanie kwasu borowego, ustalając w nich śmiertelną dawkę w 2.000 do 3.000 mg.
Bibliografia
- Shiver & Atkins. (2008). Chemia nieorganiczna. (Czwarta edycja). MC Graw Hill.
- Wikipedia. (2019). KWAS BOROWY. Źródło: w:.Wikipedia.org
- National Center for Biotechnology Information. (2019). KWAS BOROWY. Baza danych Pubchem. CID = 7628. Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov
- Redaktorzy Enyclopaedia Britannica. (28 marca 2019 r.). KWAS BOROWY. Encyclopædia Britannica. Odzyskane z: Britannica.com
- Wibracja przewoźnika. (9 listopada 2018 r.). Ukryte wyżyny kwasu burskiego w twoim codziennym życiu. Odzyskane z: przewoźnik.com
- Narodowe centrum informacji o pestycydach. (S.F.). KWAS BOROWY. Odzyskane z: NPIC.Orst.Edu
- Redakcja. (30 listopada 2017). Kwas borowy: właściwości i zastosowania tego związku chemicznego. Źródło: kwasy.Informacje
- Chlorurosod. (2019). Kwas borowy. Odzyskane z: chlorurosod.com
- Hiszpańskie społeczeństwo apteki szpitalnej. (S.F.). Kwas borowy. [PDF]. Źródło: grupy pracy.Sefh.Jest
- « Komparator optyczny, jakie jest użycie i części
- 11 Korzyści z recyklingu w społeczeństwie (z przykładami) »

