Struktura borodku sodu (NABH4), właściwości, zastosowania

- 1539
- 37
- Pani Waleria Marek
On Bor sodu Jest to nieorganiczna substancja stała, której wzorem chemicznym jest NABH4. Można go uznać za reprezentatywne dla alkalicznych borohydruros i jest najczęstszym z nich. Jest to krystaliczna biała stała.
Po kontakcie z wodą Nabh4 może generować ciepło i wodór h2 które jest paliwem, więc należy je zachować ostrożnie. Dla łatwości, z jaką może generować jony wodorku h-, Bor sodu jest umiarkowanie redukującym związkiem, więc jest szeroko stosowany w reakcjach chemicznych w tym celu.
 Borohend sodu, NABH4, solidny. Ondřej Mang [domena publiczna]. Źródło: Wikimedia Commons.
Borohend sodu, NABH4, solidny. Ondřej Mang [domena publiczna]. Źródło: Wikimedia Commons. Jego właściwość redukująca jest również stosowana w branży papierowej, ponieważ pozwala poprawić charakterystykę jasności i stabilności miazgi i papieru podczas działania przeciwko utlenianiu celulozy, głównego składnika papieru.
Ponieważ w obecności wody może łatwo tworzyć wodór, zbadano również możliwość wykorzystania go jako odwracalnego źródła wodoru w ogniwach paliwowych.
Ma inne zastosowania oparte na jego redukującej własności, na przykład w branży farmaceutycznej.
[TOC]
Struktura
Bor sodu jest związkiem jonowym. Powstaje przez anion borohydru [BH4]- wraz z kationą sodu+.
Anion [bh4]- Jest czworościenny.
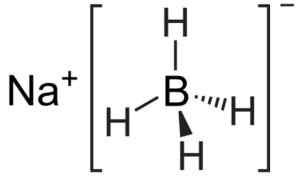 Struktura borodku sodu. Kemikungen [domena publiczna]. Źródło: Wikimedia Commons.
Struktura borodku sodu. Kemikungen [domena publiczna]. Źródło: Wikimedia Commons. Jego struktura Lewisa jest następująca:
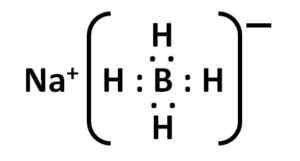 Struktura elektroniczna Nabh Lewis4. Autor: Marilú Stea.
Struktura elektroniczna Nabh Lewis4. Autor: Marilú Stea. Nomenklatura
-Bor sodu
-Tetrahydroan sodu
-Sodu tetrahydrurorat
Właściwości fizyczne
Stan fizyczny
Krystaliczna biała stała.
Waga molekularna
37,84 g/mol
Temperatura samo -kierunkowego
∼ 220 ºC
temperatura rozkładu
> 250 ° C
Gęstość
1074 g/cm3 w 20 ° C
Może ci służyć: Grignard Reagent: przygotowanie, aplikacje, przykładyRozpuszczalność
Nabh4 Jest dość rozpuszczalny w wodzie (55 g/100 ml w 25 ° C), gdzie częściowo hydrolizy. Jest rozpuszczalny w tetrahydrofurano (THF) i jest nierozpuszczalny w eterze dietedowym.
Właściwości chemiczne
Bor sodu rozpuszcza się w wodzie, gdzie cierpi początkowy rozkład lub hydrolizę, która czyni roztwór podstawowy, co zapobiega późniejszej hydrolizy.
[Bh4]- + H2O → B (OH)3 + H2↑ + OH-
Wyjaśniono to, ponieważ [bh4]- Współpracuj z h+ Wody, gdzie h+ Weź wodorość hnionu- Do utworzenia h2. Można powiedzieć, że BH3 konkuruje z h+ Dla wodorku h-.
W kwaśnej hydrolizy pożywki jest kompletna ze względu na obfitość jonów H+.
Nabh4 Jest stabilny w suchym powietrzu. To nie jest niestabilne.
Ze względu na zawartość jonów wodorkowych bor sodu jest związkiem redukującym. Pozwala na zmniejszenie grupy karbonylowej C = O A C-OH, czyli związki karbonylowe do alkoholi.
Nabh4 Sam nie zmniejsza podwójnych wiązań c = c, nawet koniugaty z grupami karbonylowymi -C = c -C (= O)-.
Jednak w kontakcie z kwasami protonowymi (takimi jak HCL) lub kwasami Lewisa (takie jak BCL3 lub ALCL3) Powstaje Diborano B2H6. A jeśli ta reakcja jest przeprowadzana w obecności związków organicznych z podwójnymi wiązaniami C = C Diborano B2H6 Wykonuje ich hydrobacion.
W obecności odpowiednich katalizatorów i określonych warunków Bor sodu może zmniejszyć różne rodzaje grup funkcjonalnych.
Ryzyko
Ciepło reakcji hydrolizy w wodzie jest wystarczające, aby włączyć utworzony w nim wodór. Dlatego ważne jest, aby zachować ostrożność podczas manipulowania.
Nabh4 Jest łatwo włączony i łatwo spalany.
Uzyskanie
Typowa reakcja przygotowania NABH4 Odbywa się przez wodorek sodu nah i b (och3)3 w temperaturze około 250 ° C:
Może ci służyć: elektroliza wody4 nah + b (och3)3 → Nabh4 + 3 Naoch3
Aplikacje
W reakcjach chemicznych redukcji
Za bycie źródłem Hones H-, Nabh4 Jest to związek redukujący i służy do przygotowania innych związków chemicznych. Aby to zrobić, jest stosowany w apratotycznych rozpuszczalnikach polarnych, to znaczy bez protonów H+, takie jak dimetylosulfotlenek, heksametylofosfal i dimetylooformamid.
Jest stosowany jako środek redukujący zarówno w reakcjach chemii organicznych, jak i nieorganicznych.
Pozwala na zmniejszenie aldehydos do pierwotnych alkoholi i ketonów do wtórnych alkoholi.
Zmniejsza również halogendy alkilowe do węglowodorów, takich jak jododan do dziekana.
Jeśli działa sam, podczas wykonywania redukcji nie wpływa na inne grupy funkcjonalne, takie jak ester, kwas karboksylowy, nitryl i sulfon.
Jego właściwość nie zmniejszania podwójnych wiązań C = C, nawet koniugaty z grupami karbonylowymi -C = C-C (= O)-, pozwala przygotować nienasycone alkohole -C = C-ch2-Oh.
W celu zmniejszenia związków aromatycznych Nitrados do odpowiednich anilinek wymaga obecności katalizatorów, takich jak chlorek kobaltu lub cyny. Zmniejsz disiarczki do tolijów.
W obecności odpowiednich warunków i katalizatorów pozwala na zmniejszenie kwasów karboksylowych, estrów, pośród azotów, iminy, epoksydów, a nawet podwójnych i potrójnych wiązań.
W h2 W ogniwach paliwowych
Nabh4 Można go zamienić w ogniwo paliwowe.
Nabh4 W obecności alkalicznego roztworu KOH lub NaOH jest on hydrolizowany i wytwarza wodór H2 które mogą być stosowane jako paliwo w polimerowej akumulatorach paliwa elektrolitu.
Został również zbadany jako materiał H do przechowywania H2 odwracalnie.
Nanocząstki NABH są syntetyzowane4 i stabilizuj za pomocą środka powierzchniowo czynnego. Po leczeniu NICL2 Powstaje warstwa ochronna lub powłoka, która reguluje uwalnianie H2 całkowicie odwracalnie.
Może ci służyć: azotan srebra (AGNO3): Struktura, właściwości, zastosowania, toksycznośćTen nowy materiał nanometryczny pozwoliłby na użycie h2 jako produkowane czyste i odnawialne paliwo.
 Pojazd, który pracuje z wodorowym ogniwem paliwowym. Dr. Artur Braun (Arturbraun) [CC BY-SA 4.0 (https: // creativeCommons.Org/licencje/nabrzeże/4.0)]. Źródło: Wikimedia Commons.
Pojazd, który pracuje z wodorowym ogniwem paliwowym. Dr. Artur Braun (Arturbraun) [CC BY-SA 4.0 (https: // creativeCommons.Org/licencje/nabrzeże/4.0)]. Źródło: Wikimedia Commons. W branży miazgi i papieru
Bor sodu służy do poprawy jasności i innych fizycznych właściwości miazgi i papieru.
Degradacja macierzy celulozowej papieru występuje poprzez złożone procesy obejmujące utlenianie. Grupy hydroksylowe utleniają karbonyl i karboksyl, prowadzi to do przebarwienia papieru i zmniejszenia właściwości fizycznych.
Podczas leczenia miazgi lub papieru NABH4, Zmniejsza to aldehydo i ketony do grup -OH bez wpływu na kwasowe grupy karboksylowe, poprawiając stabilność i jasność do wartości większych niż inicjały.
 Nabh4 pozwala na poprawę jasności papieru. Autor: Rawpixel. Źródło: Pixabay.
Nabh4 pozwala na poprawę jasności papieru. Autor: Rawpixel. Źródło: Pixabay. W kilku zastosowaniach
Bor sodu jest stosowany do leczenia ścieków, jako nieprawidłowy środek smaku w przemyśle spożywczym, jako środek powlekania oraz do obróbki powierzchni, w produkcji tytoniu, w skórze farmaceutycznej, tekstylnej i tekstylnej skóry.
Bibliografia
- Christian, m.L. i Agiey-Zinsou, K.-F. (2012). Strategia rdzeniowej prowadzącej do wysokiej odwracalnej pojemności wodoru dla NABH4. ACS Nano 2012, 6, 9, 7739-7751. Odzyskane z pubów.ACS.org.
- Nora de Souza, m.V. i Alves v., T.R. (2006). Ostatnie metodologie za pośrednictwem borohoblodku sodu w redukcji różnych klas związków. App. Organometal. Chem. 2006; 20: 798-810. Pobrano z biblioteki online.Wiley.com.
- Imamoto, t. (1991). Zmniejszenie. Borowodorek sodowy. W zrozumieniu syntezy organicznej. Odzyskane z naukowym.com.
- Tang, L.C. (1986) Stabilizacja papieru poprzez obróbkę borno -hodek sodu. W historycznych materiałach tekstylnych i papierowych. Rozdział 24. Strony 427-441. Postęp w chemii, tom 212. Odzyskane z pubów.ACS.org.
- Bawełna, f. Albert i Wilkinson, Geoffrey. (1980). Zaawansowana chemia nieorganiczna. Czwarta edycja. John Wiley & Sons.
- Morrison, Robert Thornton; i Boyd, Robert Neilson. 1992. Chemia organiczna. Prentice-Hall. ISBN 81-203-0765-8.
- LUB.S. National Library of Medicine. (2019). Borowodorek sodowy. Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov.
- « Charakterystyka i przykłady zjawiska społecznego
- Chlorek kobaltu (COCL2 (struktura, nomenklatura, właściwości »

