Charakterystyka autofagii, typy, funkcje, badania
- 3266
- 305
- Matylda Duda
Autofagia Jest to wewnątrzkomórkowy system degradacji, który występuje w zachowany sposób w lizosomach wszystkich komórek eukariotycznych (i wakuoli drożdży). Słowo jest ogólnie używane w odniesieniu do degradacji składników cytosolu lub „części” komórki, które są „przestarzałe” lub przestały działać prawidłowo.
Termin autofagia została wymyślona w 1963 roku na Uniwersytecie Rockefeller przez Duve, który również zaobserwował i opisał procesy endocytozy komórki. Dosłownie słowo autofagia oznacza „konsumowanie się”, chociaż niektórzy autorzy opisują to jako „kanibalizm samochodowy”.
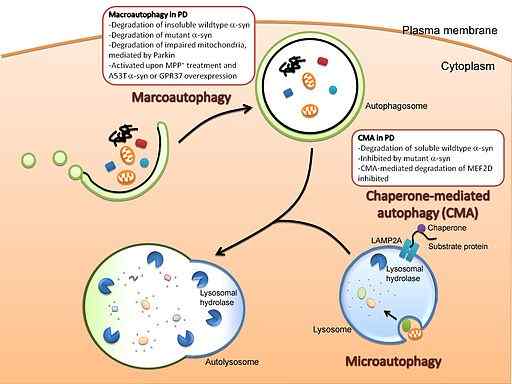
 Reprezentacja graficzna makroautofagu i mikroanofagii (źródło: Cheung i IP [CC przez 3.0 (https: // creativeCommons.Org/licencje/według/3.0)] przez Wikimedia Commons)
Reprezentacja graficzna makroautofagu i mikroanofagii (źródło: Cheung i IP [CC przez 3.0 (https: // creativeCommons.Org/licencje/według/3.0)] przez Wikimedia Commons) Ten system różni się od degradacji za pośrednictwem degradacji.
Pomimo tej nieselektywnej fagocytozy, różne badania wykazały, że autofagia ma liczne implikacje fizjologiczne i patologiczne. Ponieważ jest aktywowany w okresach adaptacji do głodu, podczas rozwoju, w celu eliminacji atakujących mikroorganizmów, podczas zaprogramowanej śmierci komórkowej, w celu eliminacji guzów, prezentacji antygenów itp.
[TOC]
Charakterystyka
Autofagia, jak wspomniano, jest procesem za pośrednictwem cytoplazmatycznej organelli znanej jako lizosom.
Proces „autofagii” rozpoczyna się od zamknięcia organelli, która zostanie zdegradowana przez podwójną błonę, tworząc błonowe ciało znane jako autofagosom. Membrana autofagosomu topi się później, z błoną lizosomalną lub późnym endosomem.
Każdy z tych etapów między porwaniem, degradacją i wyzwoleniem aminokwasów lub innych składników do recyklingu wykonuje różne funkcje w różnych kontekstach komórkowych, co sprawia, że autofagia jest wysoce wielofunkcyjnym układem.
Autofagia jest procesem dość kontrolowanym, ponieważ tylko zaznaczone składniki komórkowe są ukierunkowane na tę ścieżkę degradacji, a oznaczenie, ogólnie, podczas procesów przebudowy komórek.
Na przykład, gdy komórka wątrobowa ustanawia odpowiedź detoksykacji w odpowiedzi na leki rozpuszczalne w tłuszczach, jej gładkie retikulum endoplazmatyczne znacznie się rozprzestrzeniają, a gdy bodziec wytwarzany przez lek zmniejsza się, nadmiar gładki retikulum endoplazmatyczne jest usuwane z przestrzeni cytosolowej przez autofagię.
Indukcja autofagii
Jednym z wydarzeń, które najczęściej wyzwala procesy autofagiczne, jest głód.
Może ci służyć: egzocytoza: proces, typy, funkcje i przykładyW zależności od rozważanego organizmu różne rodzaje niezbędnych składników odżywczych mogą wywołać ten system „recyklingu”. Na przykład u drożdży, chociaż brak węgla niektórych aminokwasów i kwasów nukleinowych może indukować autofagię, brak azotu jest najbardziej wydajnym bodźcem, który jest również ważny dla komórek roślinnych.
Chociaż nie zostało to całkowicie zrozumiane, komórki mają specjalne „czujniki” w celu ustalenia, kiedy niezbędny składnik odżywczy lub aminokwas jest w bardzo niskich warunkach, a tym samym wyzwala cały proces recyklingu przez lizosomy.
U ssaków niektóre hormony uczestniczą w regulacji (pozytywnej lub ujemnej) autofagii w komórkach należących do niektórych narządów, takich jak insulina, niektóre czynniki wzrostu lub interleukiny itp.
Chłopaki
Istnieją trzy główne typy autofagii wśród eukariotów: makroautofagia, mikroanofagia i autofagia za pośrednictwem opiekuńczy. O ile nie określono, termin autofagia odnosi się do makroautofagu.
Chociaż trzy rodzaje autofagii są morfologicznie różne, wszystkie kończą się transportem substancji do lizosomów w celu ich degradacji i recyklingu.
Makroautofag
Jest to rodzaj autofagii, która zależy od treningu Novo pęcherzyków fagocytarnych zwanych autofagosomami. Tworzenie tych pęcherzyków jest niezależne od tworzenia „żółtka” błony, ponieważ są one tworzone przez rozszerzenie.
U drożdży tworzenie autofagosomów rozpoczyna się w określonym miejscu zwanym PAS, podczas gdy u ssaków występuje wiele różnych miejsc cytosolu, prawdopodobnie związanych z retikulum endoplazmatycznym poprzez struktury zwane „omegasomami”.
Wielkość autofagosomów jest bardzo zmienna i zależy od organizmu i rodzaju cząsteczki lub organulum, jaką jest fagocyt. Może się różnić od 0.4-0.O średnicy 9 μm w drożdżach do 0.5-1.5 μm u ssaków.
Kiedy membrany autofagosomowe i lizosomowe Mel. Ta organelle jest wówczas znana jako autolisosom.
W przypadku niektórych autorów makroautofaga można z kolei podklasować w indukowanej autofagii i podstawowej autofagii. Indukowany makroautofag jest stosowany do wytwarzania aminokwasów po przedłużonym okresie głodu.
Basalny makroautofag.
Może ci służyć: tratwy lipidowe: cechy, typy, funkcjeMikroanofagia
Ten rodzaj autofagii odnosi się do procesu, w którym zawartość cytoplazmatyczna jest wprowadzana do lizosomu poprzez inwazinacje występujące w błonie wspomnianej organelli.
Po wprowadzeniu do lizosomu, pęcherzyki wytwarzane przez te invaginations unoszą się swobodnie w świetle, dopóki nie zostaną wymienione, a ich zawartość zostaną zwolnione i degradowane przez określone enzymy.
Samofagia za pośrednictwem opiekuna
Ten rodzaj autofagii został zgłoszony tylko dla komórek ssaków. W przeciwieństwie do makroautofagii i mikroanofagii, gdzie niektóre porcje cytozolowe są niespecyficznie fagocytą.
Niektórzy badacze ustalili, że ten motyw pentapéptide jest związany z sekwencją Kferq i że jest on w ponad 30% białek cytozolowych.
Nazywa się to „opiekunem za pośrednictwem”, ponieważ białka opiekuńcze są odpowiedzialne za utrzymanie tego powodu zachowanego w celu ułatwienia ich rozpoznania i uniknięcia fałdowania białka.
Białka z tą etykietą są translokowane do światła lizosomalnego i są tam zdegradowane. Wiele substratów degradacji to enzymy glikolityczny.
A także pozostałe dwa rodzaje autofagii, autofagia za pośrednictwem opiekuna.
Funkcje
Jedna z głównych funkcji autofagu.
Dzięki obserwacji elektronicznych mikrofotografii lizosomów w komórkach ssaków wykryto w nich obecność peroksysomów i mitochondriów.
Na przykład w komórce wątroby średni czas życia mitochondriów wynosi 10 dni, po czym ta organelle jest fagocytowana przez lizosomy, gdzie jest degradowana, a jej składniki są recyklingowe do różnych celów metabolicznych.
Przy niskim stężeniu substancji żywieniowych komórki mogą wyzwolić tworzenie autofagosomów w celu „selektywnego wychwytywania” porcji cytosolu, a także strawione metabolity w tych autofagosomach mogą pomóc komórek przetrwać, gdy warunki zewnętrzne ograniczają się z punktu odżywczego widoku odżywczego.
Może ci służyć: erytropoiesis: etapy i jej cechy, regulacja, stymulantyFunkcje zdrowia i rozwoju
Autofagia ma ważne funkcje w restrukturyzacji komórek w procesie różnicowania, ponieważ uczestniczy w odrzucaniu części cytozolowych, które nie są wymagane w określonych czasach.
Ma również ważne implikacje w zdrowiu komórek, ponieważ jest częścią mechanizmów obronnych przed wirusami i atakującymi bakterią.
Studia Yoshinori Ohsumi
Yoshinori Ohsumi, japoński badacz w 2016 roku z Nagrodą Nobla w dziedzinie fizjologii i medycyny, opisał molekularne mechanizmy samoobrony w drożdżach, badając miejsce metaboliczne wielu białek i wakuoli tych organizmów jednokomórkowych.
W swoich pracach Ohsumi nie tylko zidentyfikował białka i trasy zaangażowane w proces, ale także wykazał, w jaki sposób trasa autofagii jest regulowana dzięki działaniu białek zdolnych do „cenzury” różnych stanów metabolicznych.
Jego praca rozpoczęła się od precyzyjnych obserwacji mikroskopowych podczas intensywnych zdarzeń degradacji. Wakuole są uważane za miejsca magazynowania „śmieci” i odpadów komórkowych z drożdży.
Obserwując drożdże z wadliwymi zmutowanymi genotypami dla różnych lub hipotetycznie genów związanych z autofagią (znaną jako geny Atg), Ten badacz i jego współpracownicy udało się opisać autofagiczny system drożdży na poziomie genetycznym.
Następnie ta grupa badaczy ustaliła główne cechy genetyczne białek kodowanych przez te geny i wniósł znaczący wkład w ich interakcję i tworzenie kompleksów odpowiedzialnych za początek i wykonanie samego siebie w drożdżach.
Dzięki pracom Yoshinori Ohsumi, dziś lepiej rozumiemy molekularne aspekty autofagii, a także jego ważne implikacje w prawidłowym funkcjonowaniu komórek i narządów, które nas tworzą.
Bibliografia
- Alberts, ur., Johnson, a., Lewis, J., Morgan, zm., Raff, m., Roberts, k., & Walter, p. (2015). Biologia komórki molekularnej (6 wyd.). Nowy Jork: Garland Science.
- Klionssky, zm. J., I emr, s. D. (2000). Autofagia jako regulowana szlak degradacji komórkowej. Nauka, 290, 1717-1721.
- Mizushima, n. (2007). Autofagia: proces i funkcja. Geny i rozwój, dwadzieścia jeden, 2861-2873.
- Mizushima, Noboru i Komatsu, M. (2011). Autostrada: odnowienie komórek i tkanek. Komórka, 147, 728-741.
- Rabinowitz, J. D., I biały i. (2010). Autofagia i metabolizm. Nauka, 330, 1344-1348.
- « Może być charakterystyk, siedlisko, reprodukcja, kontrola biologiczna
- Charakterystyka tarantula, siedlisko, gatunki, zachowanie »

