Historia sodu, struktura, właściwości, ryzyko i zastosowania

- 2900
- 258
- Bertrand Zawadzki
On sód Jest to metal alkaliczny grupy 1 stolika okresowego. Jego liczba atomowa wynosi 11 i jest reprezentowana z symbolem chemicznym Na. Jest to lekki metal, mniej gęsty niż woda, srebrna biała, która staje się szara po wystawieniu na powietrze; Dlatego jest przechowywany w parafinach lub gazach szlachetnych.
Ponadto jest to miękki metal, który można wyciąć nożem i staje się krucha w niskich temperaturach. Reaguje wybuchowo z wodą z tworzeniem wodorotlenku sodu i wodoru gazowego; Reaguje również z wilgotnym powietrzem i wilgocią nagich.
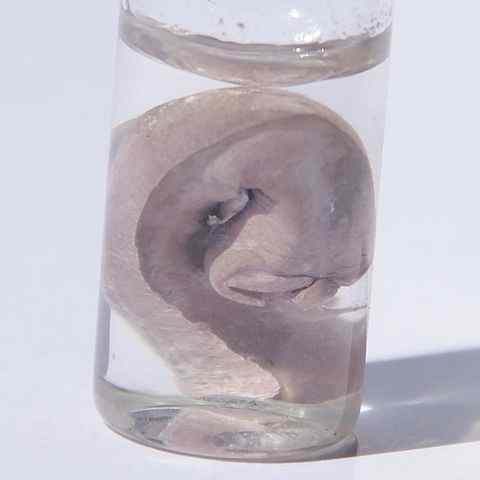 Metaliczny sód przechowywany w butelce i zanurzony w oleju, aby nie reagował z powietrzem. Źródło: obrazy Hi-Resa elementów chemicznych [CC przez 3.0 (https: // creativeCommons.Org/licencje/według/3.0)]
Metaliczny sód przechowywany w butelce i zanurzony w oleju, aby nie reagował z powietrzem. Źródło: obrazy Hi-Resa elementów chemicznych [CC przez 3.0 (https: // creativeCommons.Org/licencje/według/3.0)] Ten metal znajduje się w skałach mineralnych skalnych, takich jak halit (chlorek sodu), w Salmuelas i na morzu. Chlorek sodu reprezentuje 80% wszystkich materiałów rozpuszczonych w morzu, mając obfitość sodu 1,05%. Jest to szósty element w obfitości skorupy Ziemi.
Analiza widm światła z gwiazd pozwoliła wykryć w nich swoją obecność, w tym słońce. Podobnie, jego obecność w meteorytach została określona.
Sód jest dobrym przewodnikiem termicznym i elektrycznym, oprócz dużej pojemności absorpcji ciepła. Doświadcz zjawiska fotoelektrycznego, to znaczy jest zdolne do emisji elektronów po oświetleniu. Gdy płomień płonie, emituje intensywne żółte światło.
Stopione sód działa jako środek przenoszenia ciepła, dlatego jest stosowany jako czynnik chłodniczy w niektórych reaktorach jądrowych. Jest również stosowany jako deoksydant i reduktor metalu, więc był stosowany w oczyszczaniu metali przejściowych, takich jak tytan i cyrkon.
Sód jest głównym podatnikiem osmolarności przedziału pozakomórkowego i jego objętości. Jest również odpowiedzialny za generowanie potencjałów czynnościowych w komórkach pobudliwych i początek skurczu mięśni.
Nadmierne spożycie sodu może wytwarzać: choroby sercowo -naczyniowe, zwiększone ryzyko wypadków mózgu, osteoporoza z powodu mobilizacji wapnia kości i uszkodzenia nerek.
[TOC]
Historia
Człowiek stosował związki sodu od czasów starożytnych, zwłaszcza chlorku sodu (wspólna sól) i węglanu sodu. Znaczenie soli jest dowodem.
W średniowieczu zastosowano związek sodu z łacińską nazwą „sodanum”, co oznaczało ból głowy.
W 1807 r. Sir Humbrey Davy izolował sód przez elektrolizę wodorotlenku sodu. Davy izolował również potas, w czasie, gdy rozważali wodorotlenku sodu i wodorotlenku potasu, takiego jak substancje elementarne i nazywane stałą alkalis.
Davy w liście do przyjaciela, napisał: „Zerwałem i odkupiłem ustalone alkalis i odkryłem, że ich bazy były dwiema substancjami nowe bardzo łatwopalne substancje podobne do metali; Ale jeden z nich jest bardziej łatwopalny niż drugi i bardzo reaktywny ”.
W 1814 r. Jöns Jakob w swoim systemie symboli chemicznych użył skrótu na łacińskie słowo „natrium”, aby wywołać sód. To słowo pochodzi od egipskiej nazwy „natron” używanej do nazywania węglanu sodu.
Struktura elektroniczna i konfiguracja sodu
Metaliczny sód krystalizuje w strukturze sześciennej wyśrodkowanej na ciele (BCC). Dlatego ich atomy NA są ustawiane w kształcie kostki, z jednym zlokalizowanym w środku, a każdy z ośmioma sąsiadami.
Struktura ta charakteryzuje się najmniej gęstym ze wszystkich, co zgadza się z niską gęstością tego metalu; Tak niski, że jest wraz z litem i potasem, jedynymi metaliami, które mogą unosić się w ciekłej wodzie (oczywiście przed eksplodowaniem). Jego niska masa atomowa w odniesieniu do jego obszernego radia atomowego, również przyczynia się do tej właściwości.
Powstały link metalowy jest jednak dość słaby, jest w stanie wyjaśnić konfigurację elektroniczną:
[Ne] 3s1
Elektrony zamkniętej warstwy nie uczestniczą (przynajmniej w normalnych warunkach) w wiązaniu metalowym; Ale elektron orbitalny 3S. Atomy Na Orbital NA 3s w celu stworzenia pasma Valencia; i 3p, pusty, zespół jazdy.
Ten pasek 3s jest nasiona, a także dla niskiej gęstości szkła, sprawia, że siła rządzona przez „morze elektronów” jest słaba. W związku z tym metaliczny sód można wyciąć metalem i topi zaledwie 98ºC.
Przejścia fazowe
Kryształ sodu może doświadczać zmian w swojej strukturze poprzez doświadczanie wzrostu ciśnienia; Podczas podgrzewania jest mało prawdopodobne, aby doznało przejść fazowych ze względu na niską temperaturę topnienia.
Po rozpoczęciu przejścia fazowego zmieniają się właściwości metali. Na przykład pierwsze przejście generuje strukturę sześcienną skoncentrowaną na twarzach (FCC). Zatem mała gęsta struktura BCC jest zagęszczana na FCC poprzez naciskanie metalicznego sodu.
Może ci służyć: eter etylowyByć może nie powoduje to znacznej zmiany właściwości sodu, a nie w jego gęstości. Jednak gdy ciśnienia są bardzo wysokie, alotropy (nie polimorfy, ponieważ są czystym metalem) stają się zaskakująco w izolatorach i elektrycznych; to znaczy, nawet elektrony są ustalane w szkle jako aniony i nie krążą swobodnie.
Oprócz powyższego jego kolory również się zmieniają; Sód przestaje być szaroawy, aby stać się ciemno, czerwonawo, a nawet przezroczysty, w miarę wzrost.
Liczby utleniania
Biorąc pod uwagę orbital Valencia 3s, gdy sód traci jedyny elektron, szybko przekształca się w kationę+, który jest izolektroniczny do neonu. To znaczy zarówno na+ Ponieważ NE ma taką samą liczbę elektronów. Jeśli przyjmuje się obecność Na+ W związku mówi się, że jego liczba utleniania wynosi +1.
Chociaż jeśli nastąpi odwrotnie, to znaczy, wygrana sodowo elektron, jego wynikowa konfiguracja elektroniczna wynosi [ne] 3s2; Jest teraz izolektroniczny z magnezem, w przypadku anionów na- Nazywany Soduro. Jeśli przyjmuje się obecność Na- W związku wówczas sód będzie miał liczbę utleniania -1.
Nieruchomości
 Roztwór etylowy płonącego chlorku sodu w celu manifestowania charakterystycznego żółtego koloru płomienia dla tego metalu. Źródło: Der Messer [CC BY-SA 3.0 (https: // creativeCommons.Org/licencje/by-sa/3.0)]
Roztwór etylowy płonącego chlorku sodu w celu manifestowania charakterystycznego żółtego koloru płomienia dla tego metalu. Źródło: Der Messer [CC BY-SA 3.0 (https: // creativeCommons.Org/licencje/by-sa/3.0)] Opis fizyczny
Miękki, plastyczny, plastyczny metal.
Masa atomowa
22 989 g/mol.
Kolor
Sód to lekki srebrny metal. Genialne, gdy jesteś świeżo cięty, ale tracisz połysk, gdy jest on w kontakcie z powietrzem, stając się nieprzezroczysty. Miękkie w temperaturze, ale dość twarde w -20 ° C.
Punkt wrzenia
880 ° C.
Temperatura topnienia
97,82 ° C (prawie 98 ° C).
Gęstość
W temperaturze pokojowej: 0,968 g/cm3.
W stanie ciekłym (temperatura topnienia): 0,927 g/cm3.
Rozpuszczalność
Nierozpuszczalne w benzene, naftowej i benzynej. Rozpuszcza się w ciekłym amonie, dając niebieski roztwór. Rozpuszcza się w rtęci, tworząc amalgamat.
Ciśnienie pary
802 K Temperatura: 1 kPa; Oznacza to, że jego ciśnienie pary jest znacznie niskie nawet w wysokich temperaturach.
Rozkład
Rozkłada się gwałtownie w wodzie, tworząc wodorotlenek sodu i wodoru.
Temperatura samowystarczalności
120-125 ºC.
Breja
0,680 CP przy 100 ° C
Napięcie powierzchniowe
192 diny/cm do punktu fuzji.
Współczynnik załamania światła
4.22.
Elektronialiczność
0,93 w skali Pauling.
Energia jonizacji
Pierwsza jonizacja: 495,8 kJ/mol.
Druga jonizacja: 4.562 kJ/mol.
Trzecia jonizacja: 6.910,3 kJ/mol.
Radio atomowe
186 PM.
Radio Kowalencyjne
166 ± 21:00.
Rozszerzalność cieplna
71 µm (m · k) w 26 ° C.
Przewodność cieplna
132,3 W/m · K przy 293,15 K.
Rezystancja
4,77 × 10-8 Ω · m a 293 k.
Nomenklatura
Sód do posiadania pojedynczej liczby utleniania +1 Nazwiska jego związków, zarządzanych przez nomenklaturę zapasową, jest uproszczony, nie określając wspomnianej liczby między nawiasami i liczbami rzymskimi.
Podobnie ich nazwiska według tradycyjnej nomenklatury kończą się na sufiks -ico.
Na przykład NaCl to chlorek sodu zgodnie z nomenklaturą standardową, będąc błędnym chlorekem sodu (i). Według systematycznej nomenklatury nazywa się to również monoklorkiem sodu; i chlorek sodu, zgodnie z tradycyjną nomenklaturą. Jednak Twoją najczęstszą nazwą jest sól stołowa.
Artykuł biologiczny
Komponent osmotyczny
Sód ma stężenie zewnątrzkomórkowe 140 mmol/l, w postaci jonowej (na+). Aby utrzymać elektrooneTralność przedziału pozakomórkowego, Na+ Towarzyszy mu aniony chlorkowe (Cl-) i wodorowęglan (HCO3-), ze stężeniami 105 mmol/L i odpowiednio 25 mmol/l.
Katacja na+ Jest głównym składnikiem osmotycznym i ma największy wkład w osmolarność przedziału pozakomórkowego, tak że istnieje równa osmolarność między przedziałem zewnątrzkomórkowym i wewnątrzkomórkowym, który gwarantuje integralność przedziału wewnątrzkomórkowego.
Z drugiej strony stężenie wewnątrzkomórkowe Na+ jest 15 mmol/l. SO: dlaczego dodatkowe i wewnątrzkomórkowe stężenia Nai nie dopasowują+?
Istnieją dwa powody, dla których to się nie wydarzyło: a) Membrana plazmatyczna jest mało przepuszczalna dla Na+. b) istnienie pompy Na+-K+.
Pompa jest istniejącym układem enzymatycznym w błonie plazmatycznej, która wykorzystuje energię zawartą w ATP do przyjmowania trzech atomów Na+ i wprowadzić dwa atomy K+.
Ponadto istnieje zestaw hormonów, w tym aldosteron, który promowanie reabsorpcji nerkowej sodu gwarantuje utrzymanie zewnątrzkomórkowego stężenia sodu w odpowiednim wartości. Hormon antydiuretyczny pomaga utrzymać objętość zewnątrzkomórkową.
Produkcja potencjałów czynnościowych
Komórki pobudliwe (neurony i komórki mięśniowe) to te, które reagują na odpowiedni bodziec, tworząc potencjał impulsu działania lub nerwu. Komórki te utrzymują różnicę napięcia przez błonę plazmatyczną.
Może ci służyć: systemy materialneWnętrze komórkowe jest negatywnie naładowane w odniesieniu do zewnętrznej komórki w warunkach spoczynkowych. Biorąc pod uwagę pewien bodziec, istnieje wzrost przepuszczalności błony+ i wejdź do komórki niewielką ilość jonów Na+, powodując pozytywne ładowanie wnętrza komórki.
Powyższe jest to, co jest znane jako potencjał czynnościowy, który można rozprzestrzeniać w neuronie i jest sposobem, w jaki informacje przemieszczają się przez nie.
Gdy potencjał czynności dociera do komórek mięśniowych, stymuluje je do skurczu poprzez mniej lub bardziej złożone mechanizmy.
Podsumowując, sód jest odpowiedzialny za wytwarzanie potencjałów czynnościowych w komórkach pobudliwych i początek skurczu komórek mięśniowych.
Gdzie to się znajduje
Skorupa ziemska
Sód jest siódmym najbardziej obfitym elementem w skorupie Ziemi, co stanowi 2,8 %. Chlorek sodu jest częścią minerału Halita, który reprezentuje 80% materiału rozpuszczonego w morzu. Zawartość sodu w morzu wynosi 1,05%.
Sód jest bardzo reaktywnym elementem, dlatego nie jest rodzima ani elementarna. Występuje w rozpuszczalnych minerałach, takich jak halit lub nierozpuszczalne minerały, takie jak kreowa (aluminium i fluorek sodu) sód).
Minerał morza i halita
Oprócz ogólnie morza, Morze Martwe charakteryzuje się bardzo wysokim stężeniem różnych soli i minerałów, zwłaszcza chlorku sodu. Wielkie słone jezioro w Stanach Zjednoczonych przedstawia również wysokie stężenie sodu.
Chlorek sodu jest prawie czysty w minerałach Halita, obecny na morzu i w strukturach skalnych. ROCA lub sól mineralna jest mniej czysta niż halit, będąc w depozytach mineralnych w Wielkiej Brytanii, Francji, Niemczech, Chinach i Rosji.
Złoża soli fizjologicznej
Sól jest ekstrahowana ze złoża skały przez fragmentację skał, a następnie proces oczyszczania soli. Przy innych okazjach woda jest wprowadzana do złoża soli, aby ją rozpuścić i utworzyć solankę, która jest następnie pompowana na powierzchnię.
Sól uzyskuje się z morza w płytkich basenach znanych jako Salinas, poprzez odparowanie słoneczne. Sól uzyskana w ten sposób nazywa się sól z zatoki lub soli morskiej.
Komórka Downs
Sód został wytworzony przez węglowodanowe zmniejszenie węglanu sodu przeprowadzonego w 1.100 ° C. Obecnie jest wytwarzany przez elektrolizę stopionego chlorku sodu, przy użyciu ogniwa Downs.
Ponieważ jednak stopiony chlorek sodu ma temperaturę topnienia ~ 800 ° C, dodaje się chlorek wapnia lub węglan sodu w celu zmniejszenia temperatury topnienia do 600 ° C.
W komorze Downs katoda ma żelazo w postaci okrągłej, wokół anody węglowej. Produkty elektrolizy są oddzielone przez siatkę stalową, aby zapobiec kontaktowaniu produktów elektrolizy: sód i chlor podstawowy.
W anodzie (+) następuje następująca reakcja utleniania:
2 Cl- (L) → Cl2 (g) +2 e-
Tymczasem w katodzie (-) występuje następująca reakcja redukcji:
2 na+ (L) +2 e- → 2 Na (L)
Reakcje
Tworzenie tlenku i wodorotlenku
Jest bardzo reaktywny w powietrzu w zależności od jego wilgoci. Reaguje na tworzenie folii wodorotlenku sodu, który może pochłaniać dwutlenek węgla i wreszcie tworzyć wodorowęglan sodu.
Utlenia się w powietrzu, aby powstrzymać tlenk sodu (na2ALBO). Podczas gdy sodowy nadtlenek (nao2) Jest przygotowywany przez ogrzewanie metalicznego sodu w temperaturze 300 ° C z tlenem pod wysokim ciśnieniem.
W stanie ciekłym rozpala 125 °. Reaguje również energicznie z wodą w celu wytworzenia wodorotlenku sodu i wodoru gazowego, powodując wybuchowość reakcji. Ta reakcja jest silnie egzotermiczna.
Na +h2O → NaOH +1/2 H2 (3.367 kilokalorów/mol)
Z kwasami fluorowcowymi
Kwasy halogeniczne, takie jak kwas solowy, reagują z sodem, tworząc odpowiednie halogenki. Tymczasem jego reakcja z kwasem azotowym wytwarza azotan sodu; I z kwasem siarkowym wytwarza siarczan sodu.
Redukcje
NA zmniejsza tlenki metali przejściowych, wytwarzając odpowiednie metale podczas uwalniania ich z tlenu. Sód reaguje również z zatrzymaniem metali przejściowych, wytwarzając metale w celu utworzenia chlorku sodu i uwalniając metale.
Ta reakcja służyła do uzyskania metali przejściowych, w tym tytanu i tantalu.
Z amoniakiem
Reakcja sodu z ciekłym amoniakiem w niskiej temperaturze i powoli tworząc sodamid (nanh2) i wodór.
Na +NH3 → Nanh2 + 1/2 godz2
Może ci służyć: renio: odkrycie, właściwości, struktura, zastosowaniaPłynny amoniak służy jako rozpuszczalnik do reakcji sodu z kilkoma metaliami, w tym arsenem, teluro, antymonią i bizmutą.
Organiczny
Reaguje z alkoholami w celu produkcji alkoholi lub alcoxides:
Na +ROH → Rona +1/2 H2
Wytwarza cofanie związków organicznych, powodując powielanie liczby węgli związku:
2 Na +2 RCl → R-R +2 NaCl
Oktan może być wytwarzany przez cofnięcie bromku butanowego za pomocą sodu.
Z metali
Sód może reagować z innymi metaliami alkalicznymi, tworząc eutktykę: stop, który powstaje w niższych temperaturach niż jego składniki; Na przykład Nak, który ma procent K wynoszący 78%. Sód tworzy również stopy z berylum z niewielkim procentem pierwszego.
Metale szlachetne, takie jak złoto, srebro, platyna, palad i iridium, a także białe metale, takie jak ołów, cyna i antymon, tworzą stopnie z płynnym sodem.
Ryzyko
Jest to metal, który intensywnie reaguje z wodą. Dlatego w kontakcie z ludzkimi tkankami pokrytymi wodą może powodować poważne uszkodzenie. Produkuje przez kontakt ze skórą i oczami poważne oparzenia.
Ponadto, przez spożycie może powodować perforację przełyku i żołądka. Jednak chociaż obrażenia te są poważne, tylko niewielka część populacji jest na nie narażona.
Największe szkody, jakie może spowodować sód wynika z nadmiernego spożycia w posiłkach lub napojach wyrządzonych przez ludzi.
Ciało ludzkie wymaga spożycia sodu wynoszącego 500 mg/dzień, aby wypełnić jego funkcję w prowadzeniu nerwów, a także skurczu mięśni.
Ale znacznie większa ilość sodu jest zwykle spożywana w diecie, co powoduje wzrost stężenia w osoczu i krwi tego samego.
Może to powodować nadciśnienie tętnicze, choroby sercowo -naczyniowe i wypadki mózgu.
Hipernatremia jest również związana z wytwarzaniem osteoporozy w celu indukcji wyjścia wapnia tkanki kostnej. Nerki mają problemy z utrzymaniem stężenia normalnego sodu w osoczu pomimo ich nadmiernego spożycia, co może prowadzić do uszkodzenia nerek.
Aplikacje
Metalowy sód
Jest stosowany w metalurgii jako czynnik deoksydowy i redukcyjny w przygotowaniu wapnia, cyrkonu, tytanu i innych metali. Na przykład zmniejsz tetrachlorek tytanu (TICL4) W celu produkcji metalicznego tytanu.
Stopiony sód jest stosowany jako środek przenoszenia ciepła, więc jest stosowany jako czynnik chłodniczy w niektórych reaktorach jądrowych.
Jest stosowany jako surowiec w produkcji siarczanu laurylu sodu, głównego składnika syntetycznego detergentu. Interweniuje również w produkcji polimerów, takich jak nylon i w związkach, takich jak cyjanek i nadtlenek sodu. Również w produkcji barwników i syntezy perfum.
Sód jest stosowany w oczyszczaniu węglowodorów i nierozpuszczalnej polimeryzacji węglowodorów. Jest również stosowany w licznych redukcjach organicznych. Rozpuszczony w ciekłym amonie służy do zmniejszenia alkin do transalqueno.
Lampy pary sodu są zbudowane do publicznego oświetlenia w miastach. Dostarczają żółty kolor, podobny do obserwowanego, gdy sód jest spalany na zapocznieniach.
Sód działa jak wysyłka, która zapewnia niebieski kolor w benzofenonie, co wskazuje, że produkt w procesie wysuszania osiągnął pożądane suszenie.
Związki
Chlorek
Jest używany do przyprawiania i oszczędzania jedzenia. Elektroliza chlorku sodu wytwarza podchloryn sodu (NaOCL), stosowany w czyszczeniu domu jako chlor. Ponadto jest stosowany jako przemysłowy bieltka papierowej miazgi i tekstyliów lub w dezynfekcji wody.
Podchloryn sodu jest stosowany w niektórych preparatach leczniczych, takich jak antyseptyczny i grzybobójczy.
Węglan i wodorowęglan
Węglan sodu jest stosowany do produkcji szkła, detergentów i środków czyszczących. Monohydowany węglan sodu jest stosowany w fotografii jako składnik programistów.
Wodorowęglan sodu jest źródłem dwutlenku węgla. Z tego powodu jest stosowany w proszku do pieczenia, w musujących sole i napojach, a także w suchych gaśnicach chemicznych. Jest również stosowany w procesie garbarni i przygotowaniu wełny.
Wodorowęglan sodu jest związkiem alkalicznym, stosowanym w leczniczym leczeniu nadpoboczności żołądka i moczu.
Siarczan
Jest używany do produkcji papieru Kraft, kartonu, szkła i detergentów. Tiosiarczan sodu jest stosowany w fotografii w celu skorygowania negatywów i rozwiniętych wrażeń.
Wodorotlenek
Powszechnie nazywany żrący lub wybielaczami, jest stosowany w neutralizacji kwasów w rafinacji oleju. Reaguje z kwasami tłuszczowymi w produkcji mydła. Ponadto jest stosowany w leczeniu celulozy.
Azotan
Jest stosowany jako nawóz, który zapewnia azot, który jest składnikiem dynamitowym.
Bibliografia
- Shiver & Atkins. (2008). Chemia nieorganiczna. (Czwarta edycja). MC Graw Hill.
- Sód. (2019). Sód. Źródło: w:.Wikipedia.org
- National Center for Biotechnology Information. (2019). Sód. Baza danych Pubchem. CID = 5360545. Odzyskane z: Pubchem.NCBI.NLM.Nih.Gov
- Ganong, w. F. (2003). Fizjologia medyczna 19 wydanie. Redakcja nowoczesna instrukcja.
- Wikipedia. (2019). Sód. Źródło: w:.Wikipedia.org
- Prezydent i Fellows of Harvard College. (2019). Sól i sód. Odzyskane z: hsph.Harvard.Edu
- Redaktorzy Enyclopaedia Britannica. (7 czerwca 2019). Sód. Encyclopædia Britannica. Odzyskane z: Britannica.com
- « Historia manganu, właściwości, struktura, użycia
- Charakterystyka homopolisacharydów, struktura, funkcje, przykłady »

