Reakcja przemieszczenia

- 1920
- 85
- Eliasz Dubiel
Wyjaśniamy, jakie są reakcje przemieszczenia, typy, które istnieją i podajemy kilka przykładów
 Reakcja między metaliczną miedzią a roztworem azotanu srebra jest reakcją przemieszczenia, która wytwarza azotan miedzi (II) (który nadaje roztwór zielonkawe niebieskie zabarwienie) i metaliczne srebro, które rośnie w postaci koloru srebrnego szarego szarego
Reakcja między metaliczną miedzią a roztworem azotanu srebra jest reakcją przemieszczenia, która wytwarza azotan miedzi (II) (który nadaje roztwór zielonkawe niebieskie zabarwienie) i metaliczne srebro, które rośnie w postaci koloru srebrnego szarego szarego Jaka jest reakcja przemieszczenia?
Reakcja przemieszczenia o Reakcja zastępcza jest rodzajem reakcji chemicznej, w której atom lub niewielka grupa atomów w cząsteczce jest zastępowana lub wypierana przez inny atom lub grupę atomów.
Reakcje przemieszczenia mogą być proste lub podwójne i są bardzo powszechne w naturze. Wiele reakcji chemicznych, które widzimy dziennie, to reakcje przemieszczenia, takie jak siarczanie zacisków w akumulatorach samochodowych.
Rodzaje reakcji przemieszczenia
Istnieją dwa rodzaje reakcji przemieszczenia, proste i podwójne, które opisano poniżej wraz z niektórymi konkretnymi przykładami:
Prosta reakcja przemieszczenia
Są to reakcje przemieszczenia, w których jeden element zastępuje drugi w związku chemicznym. Są one rozpoznawane, ponieważ zarówno w odczynnikach, jak i w produktach, w których biorą udział tylko dwie substancje, aw każdym przypadku jeden z nich jest czystym elementem, podczas gdy drugi jest złożonym.
Reakcje te mogą mieć jedno z następujących ogólnych równań:
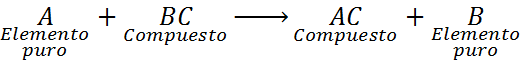
Jak widać, w tej reakcji element A reaguje ze związek BC i wypiera lub zastępuje element B, tworząc związek AC.
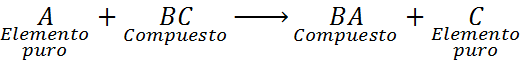
W tym przypadku element A również reaguje ze związek BC, ale wypiera lub zastępuje element C, tworząc związek BA, uwalniając C w postaci czystego elementu.
Jedną z najważniejszych cech rozpoznania prostej reakcji przemieszczenia jest to, że element przychodzący musi zajmować to samo miejsce, które zajmowało element wychodzący (B lub C, jak może być przypadek), a to musi się zakończyć jako element czysty.
Może ci służyć: galus arseniuro: struktura, właściwości, zastosowania, ryzykoNależy zauważyć, że w wielu przypadkach część C cząsteczki niekoniecznie jest elementem indywidualnym, ale może być grupą atomów, takich jak jony azotanowe (nie3-) lub siarczan (więc4-).
Przykłady prostych reakcji przemieszczenia
- Srebrne przemieszczenie miedzi
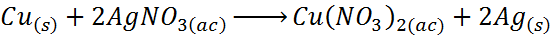
W tym przypadku miedź (Cu) działa na element A, srebro (AG) odpowiada elementowi B i jonom azotanowym (nie3-) Reprezentuj c.
Jak widać, w tej reakcji miedź zastępuje srebro w azotanie srebra, uwalniając srebro w sposób podstawowy.
- Siarczanie zacisków akumulatorowych

Ta prosta reakcja przemieszczenia dzieje się w zaciskach lub stykach elektrycznych wielu akumulatorów ołowiu, to znaczy akumulatorów obecnych w większości samochodów benzynowych.
Reakcję świadczy tworzenie białej substancji stałej, która obejmuje kontakty ołowiowe tych akumulatorów. Jak widać w równaniu, jest to reakcja, w której ołów wypiera wodór w kwasie siarkowym.
- Przemieszczenie bromu przez fluorek

W tym przypadku fluorek, który jest bardzo reaktywnym elementem, zastępuje brom w bromku sodu (NABR) z wytworzeniem fluorku sodu (NAF). Zauważ, że tutaj wymieniony element nie jest tym, który pojawia się pierwszy w wzorze złożonym, ale jest to drugi, jak w drugiej formie wcześniej pokazanej reakcji ogólnej reakcji.
Może ci służyć: destylacja ułamkowa: proces, sprzęt, aplikacje, przykładyReakcja podwójnego przemieszczenia
Reakcje podwójnego przemieszczenia, zwane także reakcjami podwójnego wymiany lub podwójnego rozkładu, można postrzegać jako wymianę par. Są to reakcje, w których dwa różne związki chemiczne wymieniają pierwiastki, tworząc dwa różne nowe związki. Reakcje te mają następujące ogólne równanie:
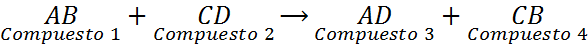
Jak widać w tej ogólnej reakcji, element A związku 1 (AB) zastępuje element związku 2 (CD) z tworzeniem związku 3 (AD). Jednocześnie element C związku 2 (Cd) zastępuje element A związku 1 (AB), tworząc związek 4 (CB).
W podwójnych przemieszczeniach istotne jest, aby elementy zastępowane ze sobą zajęły równoważne pozycje w nowych związkach. Oznacza to, że w reakcji ogólnej A, czyli po lewej stronie, a zatem jest to prawdopodobnie kation, może zastąpić tylko C w związku CD, ale nie może zastąpić D.
Jest to podobne do wymiany par tanecznych. Jeśli wszystkie pary powstają przez mężczyznę i kobietę, nowe pary utworzone po reakcji muszą być również utworzone przez mężczyznę i kobietę.
Przykłady reakcji podwójnego przemieszczenia
- Reakcja między chlorkiem sodu a azotanem srebra

Jest to wyraźny przykład reakcji podwójnego przemieszczenia. Tutaj sód zastępuje srebro w azotanie srebra, tworząc azotan sodu (nano3), W tym samym czasie, gdy srebro zastępuje sód w chlorku sodu, tworząc chlorek srebra (AGCL).
Może ci służyć: EPID- Reakcja między siarczanem wapnia a chlorkiem sodu

W tej podwójnej reakcji przemieszczenia wapń zastępuje sód w chlorku sodu, tworząc chlorek wapnia, podczas gdy sód zastępuje wapń w siarczanach wapnia, tworząc siarczan sodu.
Innym sposobem zobaczenia tej reakcji, która jest równie ważna, jest to, że siarczan zastępuje chlorek w chlorku sodu, tworząc siarczan sodu, podczas gdy chlorek zastępuje siarczan.
Chociaż obie formy są równie akceptowalne, pierwsza jest bardziej powszechna niż druga.
- Reakcja między kwasem siarkowym a wodorotlekiem potasowym
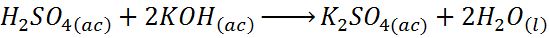
Reakcja między kwasem siarkowym a wodorotlenkiem potasowym jest reakcją neutralizacyjną opartą na kwasie zasadowym, ale jest to również reakcja podwójnego przemieszczenia.
W tym przypadku wodór zastępuje potas wodorotlenku potasu z tworzeniem wody, podczas gdy potas zastępuje wodór w kwasie siarkowym z tworzeniem siarczanu potasu.

