Radio atomowe
- 4600
- 818
- Gabriela Łuczak
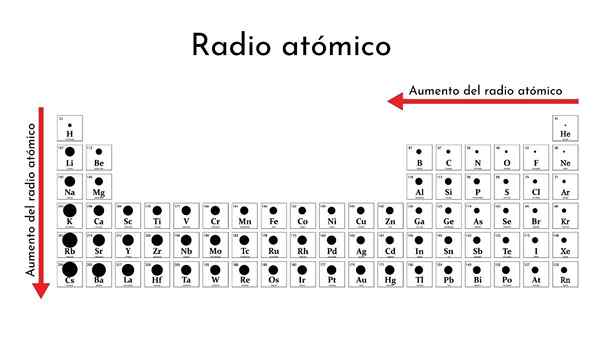
 Okresowa tabela pierwiastków z radiom atomowym
Okresowa tabela pierwiastków z radiom atomowym Co to jest radio atomowe?
On Radio atomowe Jest to ważny parametr dla właściwości okresowych elementów tabeli okresowej. Jest bezpośrednio związany z wielkością atomów, ponieważ większe radio, większe lub nieporęczne. Podobnie jest to związane z elektrycznymi charakterystykami tego samego.
Podczas gdy atom ma więcej elektronów, im większy rozmiar atomowy i radio. Oba są zdefiniowane przez elektrony warstwy Walencji, ponieważ na odległości poza ich orbitami prawdopodobieństwo znalezienia elektronu zbliża się do zera. Odwrotnie występuje w pobliżu jądra: prawdopodobieństwo znalezienia elektronu jest zwiększone.
 Pakiet bawełniany. Sposób, w jaki są kompaktowani, określa ich rozmiar i radiotelefony, w ten sam sposób, w jaki dzieje się z atomami
Pakiet bawełniany. Sposób, w jaki są kompaktowani, określa ich rozmiar i radiotelefony, w ten sam sposób, w jaki dzieje się z atomami Górny obraz reprezentuje opakowanie bawełniane. Zauważ, że każdy jest otoczony sześcioma sąsiadami, nie licząc innego możliwego lub dolnego rzędu. Sposób zagęszczania bawełnianych piłek zdefiniuje ich rozmiary, a zatem ich radia; Jak w przypadku atomów.
Pierwiastki według ich chemicznego charakteru oddziałują z ich własnymi atomami w taki czy inny sposób. Dlatego wielkość promienia atomowego zmienia się w zależności.
Jak mierzony jest promień atomowy?
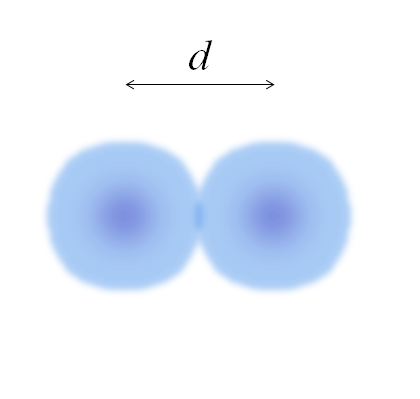 Obraz dwóch atomów, których krawędzie nie są w pełni zdefiniowane. Źródło: Gabriel Bolívar
Obraz dwóch atomów, których krawędzie nie są w pełni zdefiniowane. Źródło: Gabriel Bolívar Na poprzednim obrazie może być proste. Jednak kula atomu nie jest w pełni zdefiniowana. Ponieważ? Ponieważ elektrony krążą i rozmywają w betonowych obszarach przestrzeni: orbitale.
Dlatego atom można uznać za kulę z nieosiągalnymi krawędziami, co nie można powiedzieć na pewno, gdzie się kończą. Na przykład na obrazie górnym region środka, blisko jądra, wygląda na bardziej intensywny kolor, a jego krawędzie są zamazane.
Może ci służyć: solvationObraz reprezentuje cząsteczkę dwuatomiczną i2 (Jak CL2, H2, ALBO2, itp.). Zakładając, że atomy są ciałami sferycznymi, jeśli odległość została określona D To oddziela oba jądra w kowalencyjnym ogniku, wystarczy, aby podzielić je na dwie połówki (D/2) w celu uzyskania promienia atomowego; Mówiąc dokładniej, kowalencyjny promień E dla E2.
Co jeśli E nie utworzy kowalencyjnych więzi ze sobą, ale był to element metaliczny? Więc D Wskazałoby to liczba sąsiadów otaczających E w ich metalowej konstrukcji; to znaczy według numeru koordynacji (n.C) atomu wewnątrz opakowania (pamiętaj o bawełnianych kulkach obrazu).
Określenie odległości międzyjądrowej
Określić D, która jest odległością międzyjądrową dla dwóch atomów w cząsteczce lub opakowaniu, wymagane są techniki analizy fizycznej.
Jednym z najczęściej używanych jest dyfrakcja x -ray. Promieniuje wiązkę światła przez szkło i badany jest wzór dyfrakcji wynikający z interakcji między elektronami i promieniowaniem elektromagnetycznym.
W zależności od opakowania można uzyskać różne wzorce dyfrakcji, a zatem inne wartości D.
Jeśli atomy są „ciasne” w sieci krystalicznej, przedstawią różne wartości D w porównaniu z tymi, którzy mieliby „wygodne”.
Podobnie, te odległości międzyjądrowe mogą wahać się od wartości, więc promień atomowy faktycznie składa się ze średniej wartości takich pomiarów.
Jak odnosi się promień atomowy i liczba koordynacji? V. Goldschmidt ustanowił związek między nimi, w którym dla n.C wynosząca 12, wartość względna wynosi 1; 0.97 do opakowania, w którym atom ma n.C równa 8; 0.96, dla n.C równa 6; i 0.88 dla n.C 4.
Może ci służyć: nadanganinian sodu (namnO4): właściwości, ryzykoJednostki
Z wartości n.C równy 12, wiele tabel zostało zbudowanych, w których porównywane są radiotelefony atomowe wszystkich elementów stolika okresowego.
Ponieważ nie wszystkie elementy tworzą takie kompaktowe struktury (n.C mniej niż 12) stosuje się stosunek v. Goldschmidt, aby obliczyć ich radiotelefony i wyrazić je dla tego samego pakowania. W ten sposób pomiary radiotelefonów są znormalizowane.
Ale w jakich jednostkach są wyrażone? Biorąc pod uwagę D Ma bardzo małą wielkość, jednostki angstrom Å (10 ∙ 10-10m) lub również szeroko stosowany pikometr (10 ∙ 10-12M).
Jak zmienisz się w stole okresowym?
Przez okres
Radia atomowe określone dla pierwiastków metali nazywane są radia metali, podczas gdy dla tych elementów nie -metalowych, radiotelefonów kowalencyjnych (takich jak fosfor, p4, lub siarka, s8). Jednak między obiema rodzajami radiotelefonów istnieje bardziej widoczne rozróżnienie niż nazwa.
Od lewej do prawej w tym samym okresie jądro dodaje protony i elektrony, ale te ostatnie są ograniczone do tego samego poziomu energii (główna liczba kwantowa).
W rezultacie jądro wykonuje rosnące skuteczne obciążenie jądrowe na elektronach walencyjnych, co kurczy promień atomowy.
W ten sposób elementy niemetaliczne w tym samym okresie mają mniejsze radiotelefony atomowe (kowalencyjne).
Schodzenie przez grupę
Po zejściu przez grupę włączane są nowe poziomy energii, co pozwala elektrony mieć więcej miejsca. Zatem chmura elektroniczna obejmuje większe odległości, jej zamazane obrzeże kończy się bardziej z jądra, a zatem promień atomowy rozszerza się.
Może ci służyć: grupa hydroksylowaSkurcz Lantanidu
Elektrony warstwy wewnętrznej pomagają zabłysnąć efektywne obciążenie jądrowe na elektronach walencyjnych. Kiedy orbitale tworzące warstwy wewnętrzne mają wiele „pustych” (węzłów), podobnie jak w przypadku orbitali F, jądro zdecydowanie kurczy promień atomowy z powodu ich słabego działania tarczy.
Fakt ten jest dowodzony w skurczu Lantanid w okresie 6 tabeli okresowej. Z HF występuje znaczny skurcz iloczyn promienia atomowego orbitali F, które są „wypełnione” jako blok F: Produkowane są Lantanoides i Actinoids.
Podobny efekt można również zaobserwować w przypadku elementów bloku P od okresu 4. Tym razem produkt słabego efektu osłony orbitali d, które są wypełnione przez okresy metali przejściowych.
Przykłady radia atomowego
W okresie 2 stolika okresowej radiotelefatyczne jej pierwiastków są:
-Li: 257 PM
-BE: 112 PM
-B: 88 PM
-C: 77 PM
-N: 74 PM
-O: 66 PM
-F: 64 PM
Należy zauważyć, że metal litowy ma największy promień atomowy (257 pM), podczas gdy fluor, położony na prawym końcu tego okresu, jest najmniejszy ze wszystkich (64 pm). Promień atomowy schodzi od lewej do prawej w tym samym okresie, a wartości listy pokazują to.
Lit, tworząc wiązania metalowe, jego promień jest metaliczny; i fluor, jak wiązania kowalencyjne (F-F), jego promień jest kowalencyjny.
Co jeśli chcesz wyrażać radiotelefatyki w jednostkach Angstrom? Wystarczy podzielić je przez 100: (257/100) = 2.57Å. I tak dalej z resztą wartości.
Bibliografia
- Chemia 301. Promienie atomowe. Odzyskane z: CH301.cm.Utexas.Edu
- CK-12 Foundation (2016). Promień atomowy. Odzyskane z: chem.Librettexts.org
- Trendy w promieniach atomowych. Zaczerpnięte z: intro.Chem.OKSTATE.Edu
- Clackamas Community College (2002). Rozmiar atomowy. Źródło: DL.Clackamas.Edu
- Clark J. (2012). Promień atomowy i jonowy. Odzyskane z: chemguide.współ.Wielka Brytania
- Shiver & Atkins. (2008). Chemia nieorganiczna (wydanie czwarte, s. 1. 23, 24, 80, 169). MC Graw Hill.

