Hydrofilowe zastosowania terminu, cechy, przykłady

- 3175
- 5
- Bertrand Zawadzki
A hydrofil lub hydrofilowy Jest to segment molekularny lub związek charakteryzujący się silnym powinowactwem do rozpuszczalników wody i polarnych. Etymologicznie oznacza „miłośnicy wody”, co oznacza, że hydrofilowy będzie w stanie skutecznie rozpuszczać lub oddziaływać z cząsteczkami wody.
Dlatego substancje hydrofilowe są zwykle rozpuszczalne lub mieszane z wodą. Jednak hydrofilowość, to znaczy jego powinowactwo do wody i innego rozpuszczalnika polarnego.
 Szkło jest materiałem hydrofilowym, ponieważ łatwo się zmoczy, a krople, które są na nim osadzone. Źródło: Pexels.
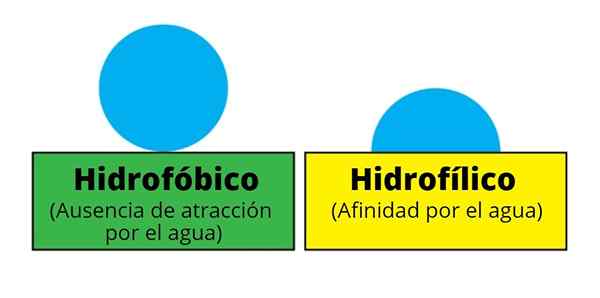
Szkło jest materiałem hydrofilowym, ponieważ łatwo się zmoczy, a krople, które są na nim osadzone. Źródło: Pexels. Zatem powierzchnie hydrofilowe są łatwiejsze do wilgocia lub zwilżenia niż hydrofobowe, te, które nienawidzą wody lub jej odpychania. Pierwsza płaska woda spada w rzędach, a te ostatnie obracają je okrągłe i widoczne. Wizualizacja tych kropli jest jednym z głównych czynników różnicowania materiału hydrofilowego od hydrofobowego.
Pojęcie hydrofilowości jest niezbędne do zrozumienia chemii powierzchni, roztworów, interfejsów i amfificznego charakteru substancji takich jak białka i kwasy tłuszczowe.
[TOC]
Zastosowanie terminu hydrofilowego lub hydrofilowego
Terminy „hydrofilowe” i „hydrofilowe” są oznaczone zarówno cząsteczek, jak i części strukturalnych tego samego. Jednak „hydrofilowy” służy głównie w odniesieniu do każdej cząsteczki lub związku, który ma duże powinowactwo do wody.
Dlatego istnieje cząsteczka hydrofilowa lub hydrofilowa, jeśli jej powinowactwo do wody jest bardzo wysokie zgodnie z pewnymi rozważaniami. Na przykład sacharoza jest hydrofilowym związkiem, który jest tym samym, co stwierdzenie, że jest hydrofilowy, ponieważ jego kryształy łatwo rozpuszczają się w dowolnej objętości wody.
Może ci służyć: TritioCząsteczka, o której mowa, może przedstawić segmenty lub części hydrofilowe, które mogą być utworzone przez karbonowany szkielet lub po prostu przez grupę polarną. Jeśli chodzi o grupę, zwykle mówimy, że jest to grupa hydrofilowa, która przyczynia się do hydrofilowości cząsteczki lub powierzchni, do której należy.
Zwykle „hydrofilowy” jest stosowany częściej niż „hydrofilowy”, ponieważ ten ostatni zwykle zastrzega się więcej niż cokolwiek innego w przypadku cząsteczek lub związków, które są całkowicie hydrofilowe; Oznacza to, że nie mają obszarów hydrofobowych w swoich strukturach molekularnych. Jest to szczególnie prawdziwe, gdy opisano makrocząsteczki lub polimerowe ciałę stałe.
Charakterystyka substancji hydrofilowych
Kowalencja
Substancje hydrofilowe to związki kowalencyjne, co oznacza, że ich jednostki składają się z cząsteczek, a nie z sieci jonowych. Dlatego chociaż sole zwykle są bardzo rozpuszczalne w wodzie, nawet więcej niż wiele hydrofilowych.
Z drugiej strony nie wszystkie sole są rozpuszczalne w wodzie, takie jak chlorek srebra, AGCL, dlatego nie można ich zaklasyfikować jako hydrofilowe.
Biegunowość
Aby cząsteczka była hydrofilowa, musi mieć pewną polarność. Jest to możliwe tylko wtedy, gdy grupy polarne, takie jak -OH, -sh, -nh mają w swojej strukturze2, -Cooh itp., tak, aby przyczyniły się do ich stałego momentu dipolowego, a zatem do ich hydrofilowości.
Interakcje
Hydrofily są rozpoznawane powyżej innych związków ze względu na ich zdolność do tworzenia mostów wodorowych za pomocą cząsteczek wody. Należy zauważyć, że wspomniane powyżej grupy polarne mają możliwość przekazywania hydrogenów lub akceptacji ich w celu utworzenia takich mostów, które są specjalnym rodzajem interakcji dipol-dipolo.
Stany stałe
Hydrofily mogą być substancje gazowe, ciekłe lub stałe, z których najczęstsze są te dwa ostatnie.
Może ci służyć: elektron różnicowyHydrofilowe płyny są mieszane z wodą, więc po jej zmieszaniu dwie fazy nie będą widoczne.
Tymczasem hydrofilowe stałe rozpuszczają się w wodzie lub bardzo łatwo ją wchłania; Ale ponadto niektórzy mają zdolność zmokania lub zmokania bez rozpuszczania się, ponieważ chociaż jej powierzchnia jest hydrofilowa, nie jest to całkiem masa wewnętrzna. Tak jest w przypadku wielu materiałów polimerowych, takich jak chemicznie zmodyfikowane silikony.
Powierzchnie hydrofilowe
Powierzchnie hydrofilowe podlegają badaniom chemii powierzchni. Nie są rozpuszczalne w wodzie, ale mogą zwilżyć i spłaszczyć krople wody, które są na niej osadzone. Jest tak, ponieważ mają zewnętrzne grupy hydrofilowe, które skutecznie oddziałują z cząsteczkami wody.
Kropla wody tworzy się z hydrofilową powierzchnią kąt kontaktu o mniej niż 90º, co jest równe, że przedstawi spłaszczony, mały sferyczny lub okrągły kształt.
Takie jest zatem, które upuszczają rozszerzanie się i działanie jak płynne rzędy. Na przykład ta właściwość służy do zapobiegania mgleniu się rozbijającym powierzchnię, ponieważ ledwo dotykana przez wodę skraplania się i zsuwa się.
Nasza skóra jest hydrofilowa, ponieważ na niej krople mają tendencję do spłaszczania i poślizgu; Z wyjątkiem sytuacji, gdy jest on zanurzony olej lub krem. Wtedy krople wody będą okrągłe i zdefiniowane, ponieważ powierzchnia stała się tymczasowo hydrofobowa.
Przykłady substancji hydrofilowych
Amoniak
Amoniak, NH3, Jest hydrofilowy, ponieważ jej cząsteczka może tworzyć kilka mostów wodorowych z wodą. To sprawia, że zarówno w stanie gazowym, jak i ciekłym jest bardzo rozpuszczalne w wodzie.
Kwas szczawiowy
Kwas szczawiowy, h2C2ALBO4, To jest hydrofil.
Może ci służyć: Petri Box: Charakterystyka, funkcje, użyj przykładówMetanol
Metanol, ch3Och, jest to hydrofilowe dzięki swojej grupie OH.
Alkohole
Alkohole są zwykle substancjami hydrofilowymi, o ile ich szkielet węglowy nie jest zbyt duży. Na przykład 1-propanol i 2-propanol są mieszane z wodą, ale nie dzieje się tak w przypadku 1-butanolu, którego mieszalność staje się niższa ze względu na jego łańcuch węglowy o większej długości.
Skrobia
Skrobia jest przykładem hydrofilowego polimeru, ponieważ jego jednostki glukozy mają wiele grup OH, z którymi mosty wodorowe tworzą się z cząsteczkami wody.
Drewno
Drewno jest hydrofilowe i chociaż nie rozpuszcza się w wodzie, szybko zwilża, jeśli nie jest obróbki powłokami hydrofobowymi.
Białka
Białka mają grupy polarne bardzo związane z wodą. Dlatego jego interakcje z cząsteczkami wody są wydajne. Nie oznacza to jednak, że wszystkie białka są rozpuszczalne w wodzie, ponieważ ich struktury (trzeciorzędne i czwartorzędowe) odgrywają fundamentalną rolę we wspomnianym procesie rozpuszczania.
Szkło
Szkło jest materiałem hydrofilowym, ponieważ chociaż nie składa się z cząsteczek, ale sieci SIO2 Trzy -wymiarowe, ich atomy tlenu mogą akceptować mosty wodorowe wodne. To jest powód, dla którego szklane naczynia się pocą w wilgotnych środowiskach.
Bibliografia
- Graham Solomons t.W., Craig b. Fryhle. (2011). Chemia organiczna. (10th Wydanie.). Wiley Plus.
- Carey f. (2008). Chemia organiczna. (Szósta edycja). MC Graw Hill.
- Morrison i Boyd. (1987). Chemia organiczna. (Piąta edycja). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Hydrofil. Źródło: w:.Wikipedia.org
- David L. Kupiec. (16 lipca 2013 r.). Wyjaśniono: hydrofobowy i hydrofilowy. Odzyskane z: wiadomości.MIT.Edu
- Najbardziej podobny. (2020). Materiały hydrofilowe. Odzyskane z:.com
- Ahmad Darem i in. (5 września 2018 r.). Materiały hydrofilowe i hydrofobowe oraz zastosowania. Taylor & Francis Online. doi.Org/10.1080/15567036.2018.1511642
- « Chaco War Tła, przyczyny, rozwój, konsekwencje
- Koncepcja obciążeń żywych, charakterystyka, przykłady »

