Typy ketonów, właściwości, nomenklatura, zastosowania, przykłady
- 647
- 20
- Arkady Sawicki
Ketony Są to związki organiczne, które mają grupę karbonylową (-co). Są to proste związki, w których karbon grupy karbonylowej jest powiązany z dwoma atomami węgla (i ich łańcuchami podstawnikowymi))). Ketony są „proste”, ponieważ nie mają grup reaktywnych, takich jak -OH lub -Cl zjednoczone z węglem.
Rozpoznawane jako związki polarne, ketony są zwykle rozpuszczalne i niestabilne, co czyni je dobrymi rozpuszczalnikami i dodatkami do perfum. Ponadto są łatwe do przygotowania, stosunkowo stabilne i mają wysoką reaktywność, co czyni je prawie idealnym związkiem pośredniego do przygotowania bardziej złożonych związków organicznych.
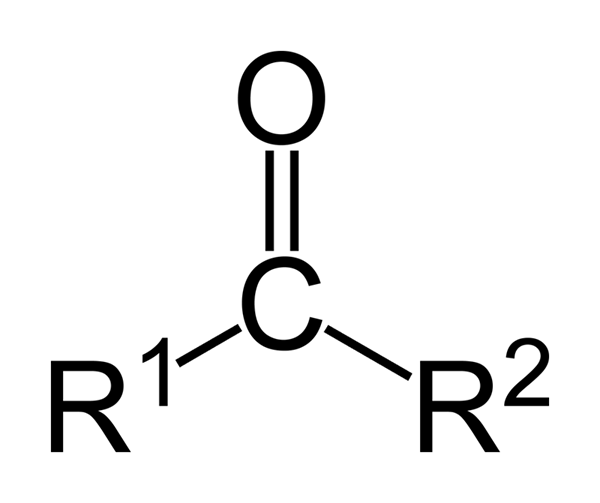
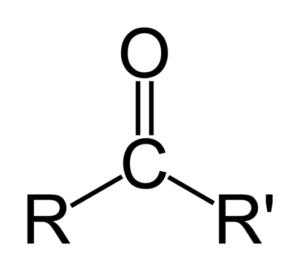
 Ogólna formuła ketonów
Ogólna formuła ketonów Wreszcie, eliminacja ketonów z ludzkiego ciała jest zwykle związana z niskim poziomem cukru (w przypadku cukrzycy i/lub ekstremalnych przypadków na czczo), co może powodować poważne problemy zdrowotne dla pacjenta.
[TOC]
Ogólna formuła ketonów
Ketony to związki karbonylowe, w których ta grupa jest powiązana z dwiema grupami węglowodorów; Mogą to być grupy alkilowe, grupy pierścieni benzenu lub oba.
Keton może być reprezentowany po prostu jako R- (C = O) -R ', gdzie R i R' są dwoma łańcuchami dowolnego węglowodoru (Alko, Alkenes, Alkines, Cycloalcanos, pochodne benzenu i innych). Nie ma ketonów z wodorem przymocowanym do grupy karbonylowej.
Istnieje wiele różnych metod przygotowywania ketonów w dziedzinie przemysłowej i laboratoryjnej; Ponadto należy zauważyć, że ketony mogą być syntetyzowane przez różne organizmy, w tym istoty ludzkie.
W branży najczęstsza metoda syntezy ketonów obejmuje utlenianie węglowodorów, zwykle przy użyciu powietrza. Na małą skalę ketony są zwykle przygotowywane przez utlenianie wtórnych alkoholi, które daje cetona i produkty wodne jako produkty.
Poza tymi najczęstszymi metodami ketony można syntetyzować przez alkeny, alkyny, sole związków azotowych, estr i wiele innych związków, co sprawia, że je łatwo uzyskane.
Rodzaje ketonów
Istnieje kilka klasyfikacji ketonów, w zależności od podstawników w ich łańcuchach R. Najczęstsze klasyfikacje tych substancji są wyznaczone poniżej:
Według struktury jego łańcucha
W tym przypadku keton jest sklasyfikowany zgodnie z ustrukturyzowanym łańcuchem: ketony alifatyczne to te, które mają dwa rodniki R i R, które mają kształt rodnika alkilowego (alkany, alkeny, alkiny i cykloalcanos).
Może ci służyć: alkohol izoamylowy: struktura, właściwości, zastosowania i ryzykoZ drugiej strony aromatyczne są te, które tworzą pochodne benzenu, a jednocześnie są ketonami. Wreszcie, mieszane ketony to te, które mają alquiliczne i radykalne r 'aril lub odwrotnie.
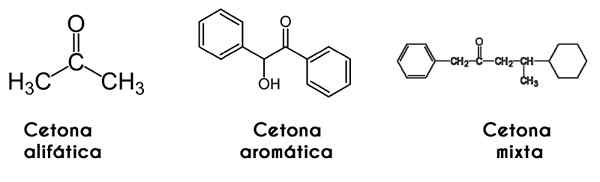 Od lewej do prawej: Propanona, Benzofrona i fenylometilbutanon. Wikimedia Commonsons Images.
Od lewej do prawej: Propanona, Benzofrona i fenylometilbutanon. Wikimedia Commonsons Images. Według symetrii ich radykałów
W tym przypadku rodniki R i R są badane przez grupę karbonylową; Kiedy są one takie same (identyczne), keton nazywa siebie symetrycznym; Ale kiedy są różne (jak większość ketonów), nazywa się asymetrycznym.
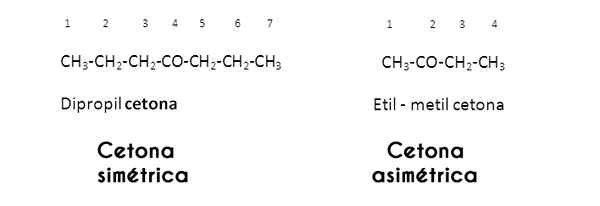 Obrazy za pośrednictwem Wikimedia Commons.
Obrazy za pośrednictwem Wikimedia Commons. Według nasycenia jego rodników
Ketony można również klasyfikować zgodnie z nasyceniem ich łańcuchów węglowych; Jeśli są one w postaci alkanów, keton nazywa siebie nasyconym ketonem. Z drugiej strony, jeśli łańcuchy są jak alkeny lub alkiny, keton nazywa się nienasycony keton.
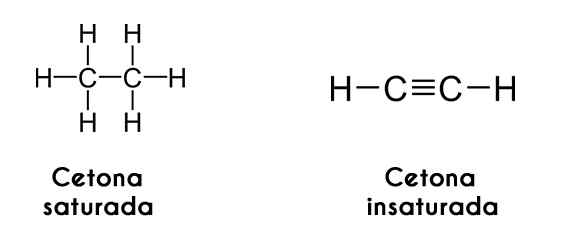 Po lewej stronie acetylen w prawo. Obrazy za pośrednictwem Wikimedia Commons.
Po lewej stronie acetylen w prawo. Obrazy za pośrednictwem Wikimedia Commons. DiceTones
Jest to klasa oprócz Cetona, ponieważ łańcuchy tego ketonu mają dwie grupy karbonylowe w swojej strukturze. Niektóre z tych ketonów mają unikalne cechy, takie jak większa długość łącza między węgle.
Na przykład dicetony pochodzące z cykloheksanu są znane jako Quinonas, które mają tylko dwa: orto-benzochinon i benzochinon.
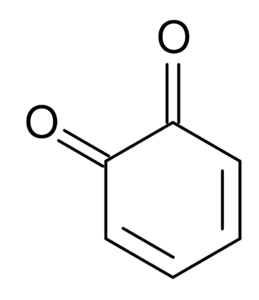 orto-benzochinon. Na południe w angielskiej Wikipedii / domenie publicznej
orto-benzochinon. Na południe w angielskiej Wikipedii / domenie publicznej Właściwości fizyczne i chemiczne ketonów
Ketony, podobnie jak większość aldehydów, są ciekłymi cząsteczkami i mają szereg właściwości fizycznych i chemicznych, które różnią się w zależności od długości ich łańcuchów. Jego właściwości opisano poniżej:
Punkt wrzenia
Ketony są wysoce lotne, znacznie polarne i nie mogą przekazywać hydrogenów wiązań wodorowych (nie mają atomów wodoru związanych z ich grupą karbonylową), więc mają wyższe temperatury wrzenia niż alkeny i etery, ale niższe niż alkohole o tej samej masie cząsteczkowej.
Temperatura wrzenia ketonu wzrasta wraz ze wzrostem wielkości cząsteczki. Wynika to z interwencji sił Van der Waalsa i Dipolo-Dipolo, które wymagają większej ilości energii do oddzielania przyciąganych atomów i elektronów w cząsteczce.
Rozpuszczalność
Rozpuszczalność ketonów ma silny wpływ w części zdolności tych cząsteczek do przyjmowania hydrogenów w ich atomie tlenu, a tym samym tworzenia wiązania wodorowego z wodą. Ponadto siły przyciągania, dyspersji i dipol-dipol między ketonami i wodą, które zwiększają ich rozpuszczalny efekt są siłami.
Może ci służyć: żelazo (element): charakterystyka, struktura chemiczna, używaKetony tracą pojemność rozpuszczalności, im większa cząsteczka, ponieważ zaczynają wymagać więcej energii do rozpuszczenia w wodzie. Są również rozpuszczalne w związkach organicznych.
Kwasowość
Dzięki grupie karbonylowej ketony mają kwaśny charakter; Dzieje się tak z powodu zdolności stabilizacji rezonansu, którą posiada ta grupa funkcjonalna, która może dać protony podwójnego wiązania, tworząc sprzężoną bazę zwaną ENOL.
Reaktywność
Ketony są częścią dużej liczby reakcji organicznych; Dzieje się tak z powodu podatności węgla karbonylowego w kierunku dodawania nukleofilowego, oprócz polaryzacji tego.
Jak wspomniano powyżej, wielka reaktywność ketonów jest wytwarzana przez rozpoznany produkt pośredni, który służy jako podstawa do syntezy innych związków.
Nomenklatura
Ketony są nazwane zgodnie z priorytetem lub znaczeniem grupy karbonylowej w całej cząsteczce, więc gdy masz cząsteczkę rządzoną przez grupę karbonylową, keton jest nazwany przez dodanie sufiks „-ona” do nazwy węglowodorów.
Zakłada się jako główny łańcuch o większej długości, jaką ma grupa karbonylowa, a następnie nazywana jest cząsteczka. Jeśli grupa karbonylowa nie ma priorytetu przed innymi grupami funkcjonalnymi cząsteczki, jest to identyfikowane z „-oxo”.
W przypadku bardziej skomplikowanych ketonów, położenie grupy funkcjonalnej można zidentyfikować z liczbą, aw przypadku dicetonów (ketony z dwoma podstawnikami R i R 'identyczne), cząsteczka jest nazwana sufiksem „-diona”.
Wreszcie, słowo „cetona” można również użyć po zidentyfikowaniu łańcuchów radykalnych powiązanych z grupą karbonylową.
Różnica między aldehydami a ketonami
Największą różnicą między aldehydami a ketonami jest obecność atomu wodoru przyłączonego do grupy karbonylowej w aldehydach.
Ten atom ma ważny wpływ, jeśli chodzi o włączenie cząsteczki w reakcji utleniania: aldehyd utworzy kwas karboksylowy lub sól kwasu karboksylowego, w zależności od utleniania w warunkach kwasowych czy podstawowych w warunkach kwasowych lub podstawowych.
Z drugiej strony Cetona nie posiada tego wodoru, więc minimalne kroki niezbędne do utleniania nie występują.
Istnieją metody utleniania ketonu (ze środkami utleniającymi znacznie silniejszą niż zwykle stosowane), ale łamie cząsteczkę cetone, dzieląc ją najpierw na dwie lub więcej części.
Może ci służyć: jonizacja w fizyce i chemii: koncepcja, proces i przykładyZastosowania życia przemysłowego i codziennego
W branży ketony są obserwowane w perfumach i obrazach, przyjmując dokumenty stabilizujące i prezerwatyw, które zapobiegają degradacji innych elementów mieszaniny; Mają także szerokie spektrum jako rozpuszczalniki w branżach, które produkują materiały wybuchowe, obrazy i tkaniny, oprócz farmaceutyki.
Aceton (najmniejszy i mniejszy keton) jest bardzo dobrze rozpoznawanym światem rozpuszczalników.
W naturze ketony mogą pojawiać się jako cukry, zwane ketusami. Ketozy to monosacharydy zawierające cetona za pomocą cząsteczki. Najbardziej znaną ketozą jest fruktoza, cukier znajdujący się w owocach i miodzie.
Biosynteza kwasów tłuszczowych występujących w cytoplazmie komórek zwierzęcych występuje również przez działanie ketonów. Wreszcie, jak wspomniano powyżej, może wystąpić wysokość ketonów we krwi po postu lub w przypadkach cukrzycowych.
Przykłady ketonów
Butanona (C4H8ALBO)
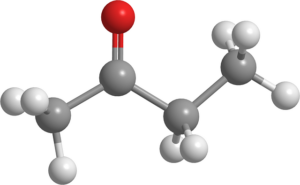 Cząsteczka Butanone. Źródło: Pixabay.
Cząsteczka Butanone. Źródło: Pixabay. Ten ciecz znany również jako MEK (lub MEC) jest produkowany na dużą skalę w branży i jest używany jako rozpuszczalnik.
Cykloheksanon (c6H10ALBO)
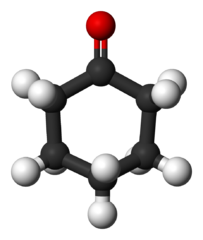 Cząsteczka cykloheksanonu. Benjah-BMM27 / Public Domena
Cząsteczka cykloheksanonu. Benjah-BMM27 / Public Domena Wyprodukowany na ogromną skalę, ten keton jest używany jako prekursor nylonowego materiału syntetycznego.
Testosteron (c19H22ALBO2)
 Cząsteczka testosteronu. Wikimedia Commons
Cząsteczka testosteronu. Wikimedia Commons Jest to główny hormon płci męskiej i steryd anaboliczny, występujący w większości kręgowców.
Progesteron (cdwadzieścia jedenH30ALBO2)
 Składnik octanu medroksyprogesteronu, cyklofemina
Składnik octanu medroksyprogesteronu, cyklofemina Endogenny steryd i hormon płciowy zaangażowany w cykl menstruacyjny, ciążę i embriogenezę u ludzi i innych gatunków.
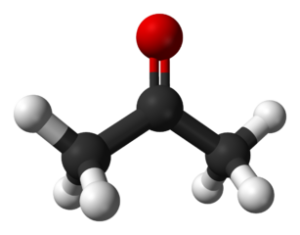
Aceton (Ch3(Co) ch3)
 Związek acetonowy. Benjah-BMM27 / Public Domena
Związek acetonowy. Benjah-BMM27 / Public Domena Znany również jako Propanona, jest to bezbarwny związek stosowany do produkcji różnych produktów przemysłowych, takich jak tworzywa sztuczne, a także do produktów higieny domowej i kosmetyków, takich jak usuwanie.
Kortyzon (cdwadzieścia jedenH28ALBO5)
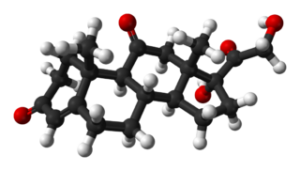 Kortyzon. Benjah-BMM27 / Public Domena
Kortyzon. Benjah-BMM27 / Public Domena Hormon steroidowy stosowany do zwalczania niektórych dolegliwości i stanów, takich jak zapalenie, trądzik, alergie i inne rodzaje reakcji skóry, astma lub rak i białaczka.
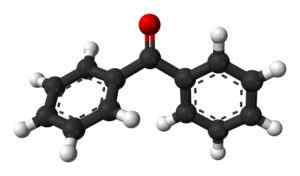
Benzofenona (c13H10ALBO)
 Benzofenoma. Benjah-BMM27 / Public Domena
Benzofenoma. Benjah-BMM27 / Public Domena Związek szeroko stosowany w tworzeniu perfum i innych produktów kosmetycznych lub przeciwsłonecznych ze względu na jego skład aromatyczny.
Bibliografia
- Wikipedia. (S.F.). Keton. Uzyskane z in.Wikipedia.org
- Britannica, e. (S.F.). Keton. Uzyskane z Britannica.com
- University, m. S. (S.F.). Aldehydes i ketony. Uzyskane z chemii.MSU.Edu
- Chemguide. (S.F.). WPROWADZENIE ALDEHYHYDY I KETONY. Uzyskane z Chemguide.współ.Wielka Brytania
- Calgary, u. ALBO. (S.F.). Ketony. Uzyskane z Chem.Ucalgary.AC

