1 z charakterystyką, syntezą, użyciem, arkusz bezpieczeństwa
- 2024
- 527
- Matylda Duda
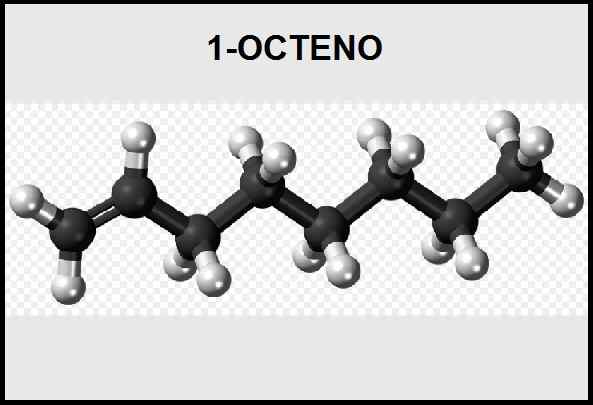
On 1-oks Jest to alken, chemikalia o charakterze organicznym, złożonym z 8-węglowego łańcucha ułożonego liniowo (alifatyczne węglowodory), z podwójnym wiązaniem między pierwszym a drugim węglem (pozycja alfa), nazywając 1-zaskarżoną.
Podwójne wiązanie sprawia, że jest to nienasycony węglowodór. Jego formuła chemiczna to c8 H16 a jego klasyczna nomenklatura to CH2 = CH-CH2-Ch2-Ch2-Ch2-Ch2-Ch3. Jest to łatwopalny związek, który musi być starannie manipulowany i wymaga przechowywania w ciemności, w temperaturze pokojowej i z dala od silnych utleniaczy i odpływów wody.
 Graficzna reprezentacja struktury chemicznej 1-okteno. Źródło: Pixabay.com. Edytowany obraz.
Graficzna reprezentacja struktury chemicznej 1-okteno. Źródło: Pixabay.com. Edytowany obraz. Synteza tego związku odbywa się za pomocą różnych metodologii, wśród najczęstszych jest oligomeryzacja etylenu i synteza fischer-tropsch. Należy zauważyć, że procedury te powodują zanieczyszczenie środowisku.
Dlatego ávila -zárraga i współpracownicy opisują, że alkeny można syntetyzować za pomocą metodologii znanej jako zielona chemia, która nie generuje odpadów, które uszkadzają środowisko.
Zapewniają również, że zastosowanie metodologii czystej lub zielonej chemii uzyskano wyższy odsetek wydajności, ponieważ badanie wykazało 7,3% procent tradycyjnej metody i 65% dla metody zielonej.
Jest stosowany jako surowiec do syntezy innych związków organicznych o ważnych zastosowaniach na poziomie branżowym. Służy również jako dodatek do żywności (aromatyzacja).
[TOC]
Charakterystyka
Chemicznie 1-okton jest zdefiniowany jako alken 8 węgli liniowych, to znaczy jest alifatycznym węglowodorem. Jest to również nienasycony węglowodór, ponieważ ma podwójne wiązanie w swojej strukturze.
Ma masę cząsteczkową 112,24 g/mol, gęstość 0,715 g/cm3, Punkt fuzji w -107 ° C, punkt zapalny 8-10 ° C, punkt samokierowania 256 ° C i temperatura wrzenia w 121 ° C. Jest to bezbarwny ciecz o charakterystycznym zapachu, nierozpuszczalnym w wodzie i rozpuszczalnym w rozpuszczalnikach nieolarnych.
Para wydana przez ten produkt jest cięższy niż powietrze, a ciecz jest gęstsza niż woda.
Synteza
Istnieje kilka metod syntezy 1-należnego, będąc wśród najbardziej znanych metodologii oligomeryzacji etylenu i syntezy fischer-tropsch.
Może ci służyć: reakcja przemieszczeniaOligomeryzacja etylenu
Oligomeryzacja etylenu jest wdrażana głównie przez ważne firmy, takie jak Shell i Chevron.
Ta technika wykorzystuje jednorodne katalizatory z metali przejściowych (katalizatory organometaliczne) wraz z ko-katalizatorami, takimi jak absolwent.
Jednak ze względu na jego wysokie koszty i zanieczyszczenie dziś środowisko, pozyskiwane są metodologie wykorzystujące heterogeniczne katalizatory w celu zminimalizowania kosztów i zmniejszenia zanieczyszczenia środowiska.
Synteza Fischer-Tropsch
Z drugiej strony synteza Fischer-Tropsch jest szeroko stosowana przez ważne firmy, takie jak SASOL (Petroprican Petroleum and Gas Petrochemical Company).
Technologia Fischer-Tropsch opiera się na transformacji gazowej (tlenek węgla i hydrogeny) w ciekłe węglowodory.
Ta reakcja wymaga interwencji katalizatorów metali oraz ciśnienia specyficznego i warunków wysokiej temperatury (150-300 ° C). Ta technika generuje mnóstwo dwutlenku siarki (więc2), tlenki azotu (NOX) i dwutlenek węgla (CO2) Dzień jako marnotrawstwo dla środowiska (wszystkie zanieczyszczenia).
Jednak jedna z najnowszych metodologii i propozycji nie.
Migdałki SSP składa się z tlenków metali, takich jak: (Sio2, 73%; Do2ALBO3, 9.1%; MGO, 2.9%; Na2Lub 1.1%; Wiara2ALBO3, 2.7%; K2Lub 1.0%; Cao, 2.0% i wujek2, 0.4%). Ta technika jest katalogowana w ramach procesów zwanych zieloną chemią. Zastępuje to kwas siarkowy i/lub kwas fosforowy.
Synteza tradycyjną metodą
a) Posiadaj bezpośredni zespół refluksowy, który jest niezbędny do przeprowadzenia procedury.
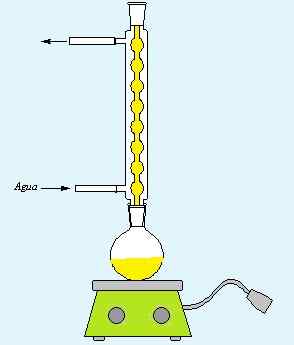 Źródło: Brak, który można odczytać, nie dostarczył autora. Zakładany Ikertza (na podstawie roszczeń dotyczących praw autorskich). [CC BY-SA 3.0 (http: // creativeCommons.Org/licencje/by-sa/3.0/]]. Edytowany obraz.
Źródło: Brak, który można odczytać, nie dostarczył autora. Zakładany Ikertza (na podstawie roszczeń dotyczących praw autorskich). [CC BY-SA 3.0 (http: // creativeCommons.Org/licencje/by-sa/3.0/]]. Edytowany obraz. b) W kolbie wydawanej 25 ml 98% kwasu siarkowego lub 85% kwasu fosforowego z 4 ml oktanolu.
c) Rozwiązania są mieszane z pomocą grilla z pobudzeniem i ogrzewaniem.
d) przez okres 90 minut ogrzewania do refluksu.
e) Włącz frakcyjny sprzęt do destylacji.
f) Podnieś temperaturę umiarkowanie i zbierz destylat w odpowiednim pojemniku (Erlenmeyer Matraz), chłodzi w kąpieli lodowej.
Może ci służyć: nienasycone rozwiązanieg) Wyjmij ze źródła ciepła, gdy w kolbie znajduje się niewielka płynna pozostałość lub gdy obserwuje się emisję białych oparów wytwarzanych przez rozkład mieszanki reakcyjnej.
h) Chlorek sodu służy do nasycenia destylatu, a następnie dekantu za pomocą lejka separacji.
i) Wykonaj 3 pranie z 5 ml 5% wodorowęglanu sodu przy każdej okazji.
j) Zbierz fazę organiczną w kolbie, a następnie umieść w kąpieli lodowej, aby się ochłodzić.
k) Następnie do wyschnięcia stosuje się bezwodny siarczan sodu. Następnie uzyskana faza organiczna odpowiada alkenowi (ośmianowi).
l) Otrzymana czarna ciekła resztę jest iloczynem rozkładu materii organicznej, należy ją leczyć podstawowymi roztworami zneutralizacji pH.
Synteza metodą zieloną
a) Włącz zespół refluksowy.
b) W kolbie wydawającej 4,8 ml oktanolu i 0,24 katalizatora (migdałki SSP).
c) Rozwiązania są mieszane z pomocą grilla z pobudzeniem i ogrzewaniem.
d) przez okres 90 minut ogrzewania do refluksu.
e) Włącz frakcyjny sprzęt do destylacji.
f) Podnieś temperaturę umiarkowanie i zbierz destylat w odpowiednim pojemniku (Erlenmeyer Matraz), chłodzi w kąpieli lodowej.
g) Wyjmij ze źródła ciepła, gdy w kolbie znajduje się niewielka płynna pozostałość i katalizator.
h) Siarczan sodu służy do wysuszenia destylatu. Następnie dekant za pomocą lejka separacji. Otrzymana faza organiczna odpowiada alkene (Octeno).
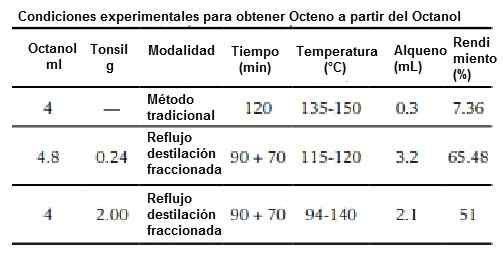 Źródło: Ávila-Zárraga G, Cano S, Gavilán-García I. Zielona chemia, uzyskiwanie alkenów stosujących zasady zielonej chemii edu. Chem, 2010; 21 (2), 183-189. Dostępne na: Scielo.org.
Źródło: Ávila-Zárraga G, Cano S, Gavilán-García I. Zielona chemia, uzyskiwanie alkenów stosujących zasady zielonej chemii edu. Chem, 2010; 21 (2), 183-189. Dostępne na: Scielo.org. Używać
1-Thorage zachowuje się jak komonomer, to znaczy jest monomer, który polimeryzuje z innymi monomerami innych niż on, nawet o zdolności polimeryzacji wobec siebie.
W ten sposób ten produkt jest przydatny w opracowaniu innych substancji o charakterze organicznym, takich jak polietylen i środki powierzchniowo czynne o niskiej gęstości.
Może ci służyć: kwas benzyny: synteza, transpozycja i zastosowaniaZ drugiej strony jest to ważny związek w niezbędnym łańcuchu reakcji w celu uzyskania liniowej aldehydo C9. Są one następnie przekształcane przez reakcje utleniania i uwodornienia w alkohol tłuszczowy (1-nonanol), stosowany jako plastyfikacja.
1 kolna jest wykorzystywana jako aromatyzowanie, a zatem jest dodawana do niektórych pokarmów w Stanach Zjednoczonych.
Arkusz bezpieczeństwa
1-octura jest substancją bardzo łatwopalną, mieszanina ich oparów z innymi substancjami może wygenerować eksplozję. Wzywając zapobieganie, należy unikać użycia sprężonego powietrza w celu manipulowania tą substancją. Musi być również trzymany w środowisku i iskry bez ognia. W przypadku pożaru za pomocą suchego pyłu, dwutlenku węgla lub pianki, aby wyłączyć płomienie.
Substancję należy zmanipulować za pomocą sukni, rękawiczek i soczewek bezpieczeństwa oraz pod dzwonem do wydobywania pary.
Wdychanie produktu powoduje senność i zawroty głowy. W bezpośrednim kontakcie wytwarza suchość skóry. W przypadku kontaktu skóry lub śluzu zaleca się mycie dotkniętego obszaru z dużą ilością. W przypadku spożycia w dużych ilościach idź do lekarza i nie powodować wymiotów.
Produkt ten musi być przechowywany w temperaturze pokojowej, z dala od silnych utleniaczy, chroniony przed światłem i daleko od odpływach wodnych.
W przypadku rozlania należy go zebrać za pomocą materiału chłonnego, na przykład piasku. Ten produkt nie powinien być wykluczony w kanałach, drenażach lub w żaden inny sposób, który wpływa na środowisko, ponieważ jest toksyczny dla życia wodnego.
Bibliografia
- Ávila-Zárraga G, Cano S, Gavilán-García I. Zielona chemia, uzyskiwanie alkenów stosujących zasady zielonej chemii Edukacja. Chem, 2010; 21 (2), 183-189. Dostępne na: Scielo.org.
- WIKPEDIA Współ, Wikipedia, wolna encyklopedia,11 czerwca 2019, 22:43 UTC, dostępny pod adresem: org
- Moussa s. Oligomeryzacja etylenu na heterogenicznych katalizatorach Ni-cheeta. Wstępne badanie kinetyczne. Instytut technologii chemicznej. Valencia Polytechnic University. Dostępne na: /riunet.UPV.Jest/
- National Institute for Work Health and Health. Rząd Hiszpanii. 1-oks. Dostępne na: ILO.org/
- Wspólny program FAO/WHO na temat standardów żywnościowych Komitet ds. Dodatków żywnościowych. Propozycje dodawania i zmian na liście priorytetów dodatków żywnościowych zaproponowanych do oceny przez JECFA. 45a Pekin Spotkanie (Chiny), 18–22 marca 2013 r. Dostępne na: FAO.org/
- « Charakterystyka gleby aluwialnej, geologia, właściwości, zastosowania
- Co to jest hałas semantyczny? (Z przykładami) »

